ПОДПИСАТЬСЯ НА РАССЫЛКУ
Биохимия печени
Тема: "БИОХИМИЯ ПЕЧЕНИ"
1. Химический состав печени: содержание гликогена, липидов, белков, минеральный состав.
2. Роль печени в углеводном обмене: поддержание постоянной концентрации глюкозы, синтез и мобилизация гликогена, глюконеогенез, основные пути превращения глюкозо-6-фосфата, взаимопревращения моносахаридов.
3. Роль печени в обмене липидов: синтез высших жирных кислот, ацилглицеролов, фосфолипидов, холестерола, кетоновых тел, синтез и обмен липопротеинов, понятие о липотропном эффекте и липотропных факторах.
4. Роль печени в белковом обмене: синтез специфических белков плазмы крови, образование мочевины и мочевой кислоты, холина, креатина, взаимопревращения кетокислот и аминокислот.
5. Метаболизм алкоголя в печени, жировое перерождение печени при злоупотреблении алкоголем.
6. Обезвреживающая функция печени: стадии (фазы) обезвреживания токсических веществ в печени.
7. Обмен билирубина в печени. Изменения содержания желчных пигментов в крови, моче и кале при различных видах желтух (надпечёночной, паренхиматозной, обтурационной).
8. Химический состав желчи и её роль; факторы, способствующие образованию желчных камней.
31.1. Функции печени.
Печень является органом, занимающим уникальное место в обмене веществ. В каждой печёночной клетке содержится несколько тысяч ферментов, катализирующих реакции многочисленных метаболических путей. Поэтому печень выполняет в организме целый ряд метаболических функций. Важнейшими из них являются:
- биосинтез веществ, которые функционируют или используются в других органах. К этим веществам относятся белки плазмы крови, глюкоза, липиды, кетоновые тела и многие другие соединения;
- биосинтез конечного продукта азотистого обмена в организме - мочевины;
- участие в процессах пищеварения - синтез желчных кислот, образование и экскреция желчи;
- биотрансформация (модификация и конъюгация) эндогенных метаболитов, лекарственных препаратов и ядов;
- выделение некоторых продуктов метаболизма (желчные пигменты, избыток холестерола, продукты обезвреживания).
31.2. Роль печени в обмене углеводов.
Основная роль печени в обмене углеводов заключается в поддержании постоянного уровня глюкозы в крови. Это осуществляется путём регуляции соотношения процессов образования и утилизации глюкозы в печени.
В клетках печени содержится фермент глюкокиназа, катализирующий реакцию фосфорилирования глюкозы с образованием глюкозо-6-фосфата. Глюкозо-6-фосфат является ключевым метаболитом углеводного обмена; основные пути его превращения представлены на рисунке 1.
31.2.1. Пути утилизации глюкозы. После приёма пищи большое количество глюкозы поступает в печень по воротной вене. Эта глюкоза используется прежде всего для синтеза гликогена (схема реакций приводится на рисунке 2). Содержание гликогена в печени здоровых людей обычно составляет от 2 до 8% массы этого органа.
Гликолиз и пентозофосфатный путь окисления глюкозы в печени служат в первую очередь поставщиками метаболитов-предшественников для биосинтеза аминокислот, жирных кислот, глицерола и нуклеотидов. В меньшей степени окислительные пути превращения глюкозы в печени являются источниками энергии для обеспечения биосинтетических процессов.
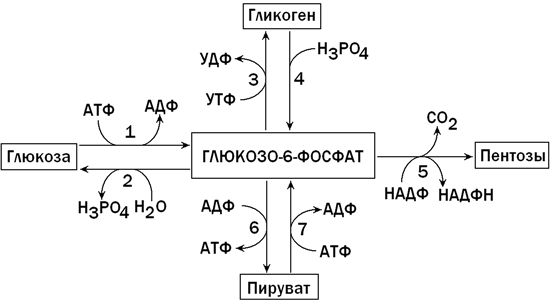
Рисунок 1. Главные пути превращения глюкозо-6-фосфата в печени. Цифрами обозначены: 1 - фосфорилирование глюкозы; 2 - гидролиз глюкозо-6-фосфата; 3 - синтез гликогена; 4 - мобилизация гликогена; 5 - пентозофосфатный путь; 6 - гликолиз; 7 - глюконеогенез.
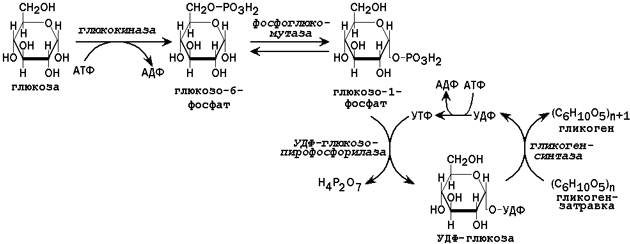
Рисунок 2. Схема реакций синтеза гликогена в печени.
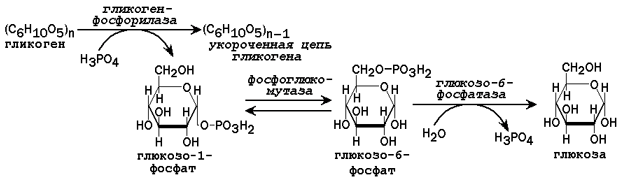
Рисунок 3. Схема реакций мобилизации гликогена в печени.
31.2.2. Пути образования глюкозы. В некоторых условиях (при голодании низкоуглеводной диете, длительной физической нагрузке) потребность организма в углеводах превышает то количество, которое всасывается из желудочно-кишечного тракта. В таком случае образование глюкозы осуществляется с помощью глюкозо-6-фосфатазы, катализирующей гидролиз глюкозо-6-фосфата в клетках печени. Непосредственным источником глюкозо-6-фосфата служит гликоген. Схема мобилизации гликогена представлена на рисунке 3.
Мобилизация гликогена обеспечивает потребности организма человека в глюкозе на протяжении первых 12 - 24 часов голодания. В более поздние сроки основным источником глюкозы становится глюконеогенез - биосинтез из неуглеводных источников.
Основными субстратами для глюконеогенеза служат лактат, глицерол и аминокислоты (за исключением лейцина). Эти соединения сначала превращаются в пируват или оксалоацетат - ключевые метаболиты глюконеогенеза.
Глюконеогенез - процесс, обратный гликолизу. При этом барьеры, создаваемые необратимыми реакциями гликолиза, преодолеваются при помощи специальных ферментов, катализирующих обходные реакции (см. рисунок 4).
Из других путей обмена углеводов в печени следует отметить превращение в глюкозу других пищевых моносахаридов - фруктозы и галактозы.
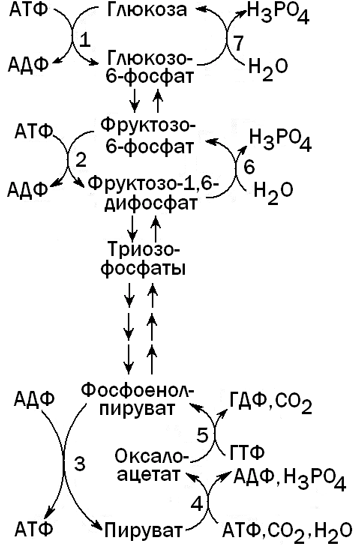
Рисунок 4. Гликолиз и глюконеогенез в печени.
Ферменты, катализирующие необратимые реакции гликолиза: 1 - глюкокиназа; 2 - фосфофруктокиназа; 3 - пируваткиназа.
Ферменты, катализирующие обходные реакции глюконеогенеза: 4 -пируваткарбоксилаза; 5 - фосфоенолпируваткарбоксикиназа; 6 -фруктозо-1,6-дифосфатаза; 7 - глюкозо-6-фосфатаза.
31.3. Роль печени в обмене липидов.
В гепатоцитах содержатся практически все ферменты, участвующие в метаболизме липидов. Поэтому паренхиматозные клетки печени в значительной степени контролируют соотношение между потреблением и синтезом липидов в организме. Катаболизм липидов в клетках печени протекает главным образом в митохондриях и лизосомах, биосинтез - в цитозоле и эндоплазматическом ретикулуме. Ключевым метаболитом липидного обмена в печени является ацетил-КоА, главные пути образования и использования которого показаны на рисунке 5.
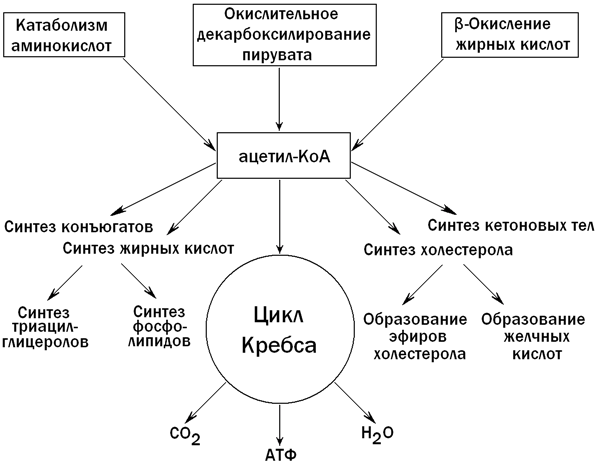
Рисунок 5. Образование и использование ацетил-КоА в печени.
31.3.1. Метаболизм жирных кислот в печени. Пищевые жиры в виде хиломикронов поступают в печень через систему печёночной артерии. Под действием липопротеинлипазы, находящейся в эндотелии капилляров, они расщепляются до жирных кислот и глицерола. Жирные кислоты, проникающие в гепатоциты, могут подвергаться окислению, модификации (укорочению или удлинению углеродной цепи, образованию двойных связей) и использоваться для синтеза эндогенных триацилглицеролов и фосфолипидов.
31.3.2. Синтез кетоновых тел. При β-окислении жирных кислот в митохондриях печени образуется ацетил-КоА, подвергающийся дальнейшему окислению в цикле Кребса. Если в клетках печени имеется дефицит оксалоацетата (например, при голодании, сахарном диабете), то происходит конденсация ацетильных групп с образованием кетоновых тел (ацетоацетат,β-гидроксибутират, ацетон). Эти вещества могут служить энергетическими субстратами в других тканях организма (скелетные мышцы, миокард, почки, при длительном голодании - головной мозг). Печень не утилизирует кетоновые тела. При избытке кетоновых тел в крови развивается метаболический ацидоз. Схема образования кетоновых тел - на рисунке 6.

Рисунок 6. Синтез кетоновых тел в митохондриях печени.
31.3.3. Образование и пути использования фосфатидной кислоты. Общим предшественником триацилглицеролов и фосфолипидов в печени является фосфатидная кислота. Она синтезируется из глицерол-3-фосфата и двух ацил-КоА - активных форм жирных кислот (рисунок 7). Глицерол-3-фосфат может образоваться либо из диоксиацетонфосфата (метаболит гликолиза), либо из свободного глицерола (продукт липолиза).
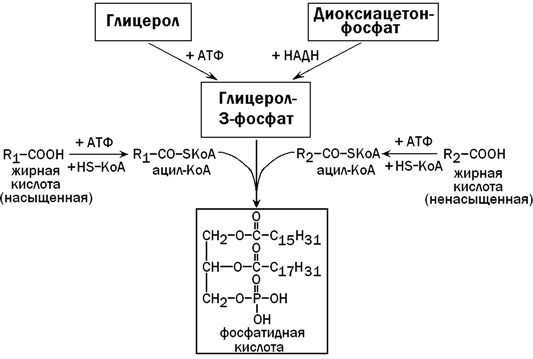
Рисунок 7. Образование фосфатидной кислоты (схема).
Для синтеза фосфолипидов (фосфатидилхолина) из фосфатидной кислоты необходимо поступление с пищей достаточного количества липотропных факторов (веществ, препятствующих развитию жировой дистрофии печени). К этим факторам относятся холин, метионин, витамин В12, фолиевая кислота и некоторые другие вещества. Фосфолипиды включаются в состав липопротеиновых комплексов и принимают участие в транспорте липидов, синтезированных в гепатоцитах, в другие ткани и органы. Недостаток липотропных факторов (при злоупотреблении жирной пищей, хроническом алкоголизме, сахарном диабете) способствует тому, что фосфатидная кислота используется для синтеза триацилглицеролов (нерастворимых в воде). Нарушение образования липопротеинов приводит к тому, что избыток ТАГ накапливается в клетках печени (жировая дистрофия) и функция этого органа нарушается. Пути использования фосфатидной кислоты в гепатоцитах и роль липотропных факторов показаны на рисунке 8.
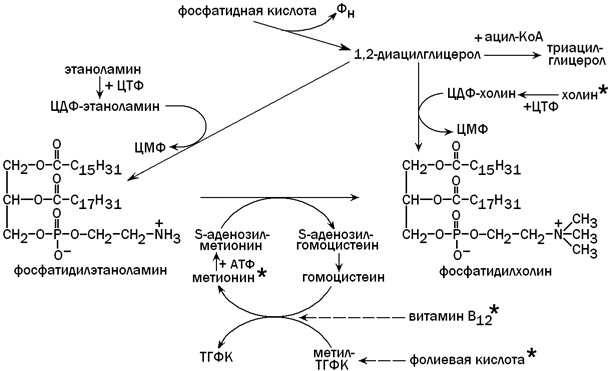
Рисунок 8. Использование фосфатидной кислоты для синтеза триацилглицеролов и фосфолипидов. Липотропные факторы обозначены знаком * .
31.3.4. Образование холестерола. Печень является основным местом синтеза эндогенного холестерола. Это соединение необходимо для построения клеточных мембран, является предшественником желчных кислот, стероидных гормонов, витамина Д3. Первые две реакции синтеза холестерола напоминают синтез кетоновых тел, но протекают в цитоплазме гепатоцита. Ключевой фермент синтеза холестерола - β-гидрокси-β-метилглутарил-КоА-редуктаза (ГМГ-КоА-редуктаза)ингибируется избытком холестерола и желчными кислотами по принципу отрицательной обратной связи (рисунок 9).
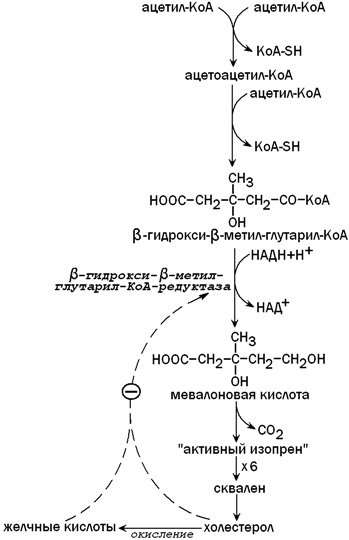
Рисунок 9. Синтез холестерола в печени и его регуляция.
31.3.5. Образование липопротеинов. Липопротеины - белково-липидные комплексы, в состав которых входят фосфолипиды, триацилглицеролы, холестерол и его эфиры, а также белки (апопротеины). Липопротеины транспортируют нерастворимые в воде липиды к тканям. В гепатоцитах образуются два класса липопротеинов - липопротеины высокой плотности (ЛПВП) и липопротеины очень низкой плотности (ЛПОНП).
31.4. Роль печени в обмене белков.
Печень является органом, регулирующим поступление азотистых веществ в организм и их выведение. В периферических тканях постоянно протекают реакции биосинтеза с использованием свободных аминокислот, либо выделение их в кровь при распаде тканевых белков. Несмотря на это, уровень белков и свободных аминокислот в плазме крови остаётся постоянным. Это происходит благодаря тому, что в клетках печени имеется уникальный набор ферментов, катализирующих специфические реакции обмена белков.
31.4.1. Пути использования аминокислот в печени. После приёма белковой пищи в клетки печени по воротной вене поступает большое количество аминокислот. Эти соединения могут претерпевать в печени ряд превращений, прежде чем поступить в общий кровоток. К этим реакциям относятся (рисунок 10):
а) использование аминокислот для синтеза белков;
б) трансаминирование - путь синтеза заменимых аминокислот; осуществляет также взаимосвязь обмена аминокислот с глюконеогенезом и общим путём катаболизма;
в) дезаминирование - образование α-кетокислот и аммиака;
г) синтез мочевины - путь обезвреживания аммиака (схему см. в разделе "Обмен белков");
д) синтез небелковых азотсодержащих веществ (холина, креатина, никотинамида, нуклеотидов и т.д.).
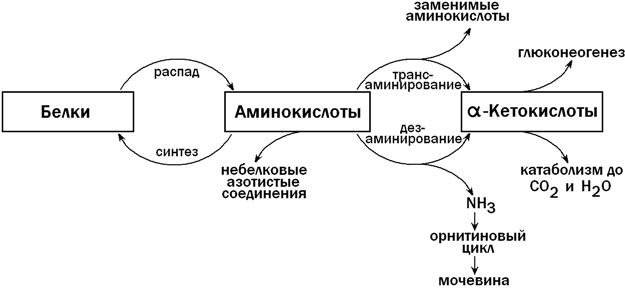
Рисунок 10. Обмен аминокислот в печени (схема).
31.4.2. Биосинтез белков. В клетках печени синтезируются многие белки плазмы крови: альбумины (около 12 г в сутки), большинство α- и β-глобулинов, в том числе транспортные белки (ферритин, церулоплазмин, транскортин, ретинолсвязывающий белок и др.). Многие факторы свёртывания крови (фибриноген, протромбин, проконвертин, проакцелерин и др.) также синтезируются в печени.
31.5. Обезвреживающая функция печени.
В печени обезвреживаются неполярные соединения различного происхождения, в том числе эндогенные вещества, лекарственные препараты и яды. Процесс обезвреживания веществ включает две стадии (фазы):
1) фаза модификации - включает реакции окисления, восстановления, гидролиза; для ряда соединений необязательна;
2) фаза конъюгации - включает реакции взаимодействия веществ с глюкуроновои и серной кислотами, глицином, глутаматом, таурином и другими соединениями.
Более подробно реакции обезвреживания будут рассмотрены в разделе "Биотрансформация ксенобиотиков".
31.6. Желчеобразовательная функция печени.
Желчь - жидкий секрет желтовато-коричневого цвета, выделяемый печёночными клетками (500-700 мл в сутки). В состав желчи входят: желчные кислоты, холестерол и его эфиры, желчные пигменты, фосфолипиды, белки, минеральные вещества (Nа+, К+, Са2+, Сl-) и вода.
31.6.1. Желчные кислоты. Являются продуктами метаболизма холестерола, образуются в гепатоцитах. Различают первичные (холевая, хенодезоксихолевая) и вторичные (дезоксихолевая, литохолевая) желчные кислоты. В желчи присутствуют главным образом желчные кислоты, конъюгированные с глицином или таурином (например, гликохолевая, кислота, таурохолевая кислота и т.д.).
Желчные кислоты принимают непосредственное участие в переваривании жиров в кишечнике:
- оказывают на пищевые жиры эмульгирующее действие;
- активируют панкреатическую липазу;
- способствуют всасыванию жирных кислот и жирорастворимых витаминов;
- стимулируют перистальтику кишечника.
При нарушении оттока желчи желчные кислоты проникают в кровь и мочу.
31.6.2. Холестерол. С желчью выводится из организма избыток холестерола. Холестерол и его эфиры присутствуют в желчи в виде комплексов с желчными кислотами (холеиновые комплексы). При этом отношение содержания желчных кислот к содержанию холестерола (холатный коэффициент) должно быть не ниже 15. В противном случае нерастворимый в воде холестерол выпадает в осадок и откладывается в виде камней желчного пузыря (желчно-каменная болезнь).
31.6.3. Желчные пигменты. Из пигментов в желчи преобладает конъюгированный билирубин (моно- и диглюкуронид билирубина). Он образуется в клетках печени в результате взаимодействия свободного билирубина с УДФ-глюкуроновой кислотой. При этом снижается токсичность билирубина и увеличивается его растворимость в воде; далее конъюгированный билирубин секретируется в желчь. При нарушении оттока желчи (механическая желтуха) в крови значительно увеличивается содержание прямого билирубина, в моче обнаруживается билирубин, в кале и моче снижено содержание стеркобилина. Дифференциальную диагностику желтух см. в разделе "Обмен сложных белков".
31.6.4. Ферменты. Из ферментов, обнаруженных в желчи, следует в первую очередь отметить щелочную фосфатазу. Это экскреторный фермент, синтезируемый в печени. При нарушении оттока желчи активность щелочной фосфатазы в крови возрастает.
ОБНОВЛЕНИЯ
ПОДПИСАТЬСЯ НА РАССЫЛКУ
ПРЕДМЕТЫ
- Анатомия
- Акушерство и гинекология
- БЖД, медицина катастроф
- Биохимия
- Биология
- Гистология
- Гигиена
- Генетика
- Диетология
- Дерматовенерология
- Инфекционные болезни
- Культурология
- Лабораторная диагностика
- Летняя практика
- Лучевая диагностика
- Медицинская информатика
- Микробиология
- Неврология
- Общественное здоровье
- Общий уход
О НАС
«Dendrit» - информационный портал для медицинских работников, студентов медицинских ВУЗов, исследователей и пациентов.
Ваш источник новостей и знаний о здоровье.