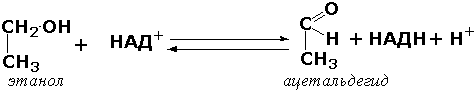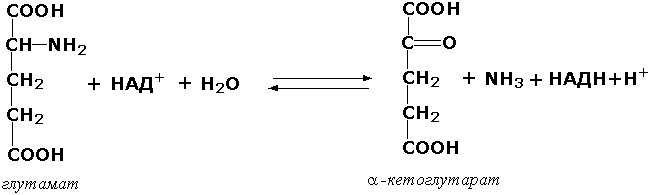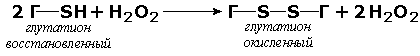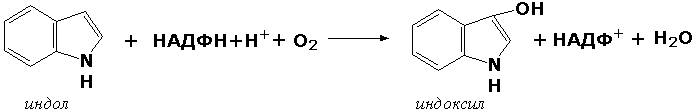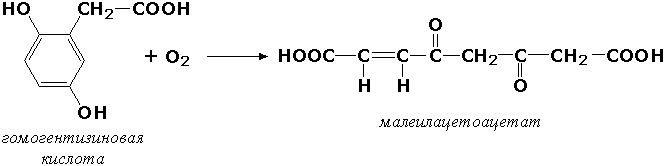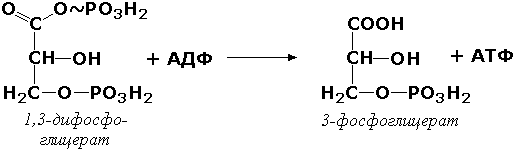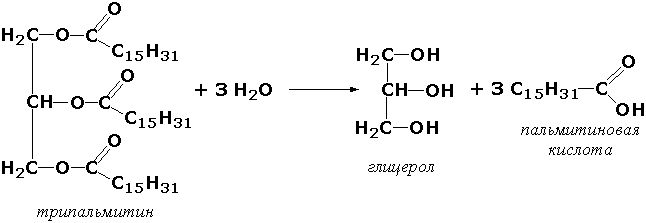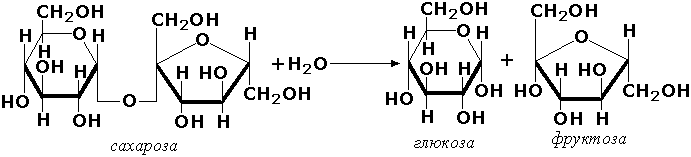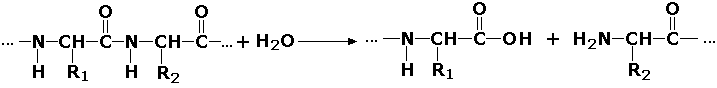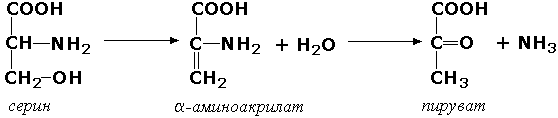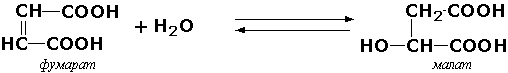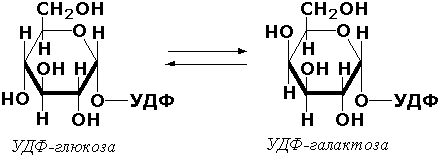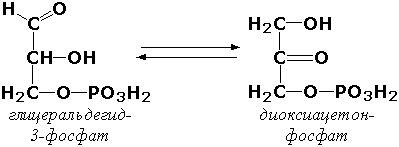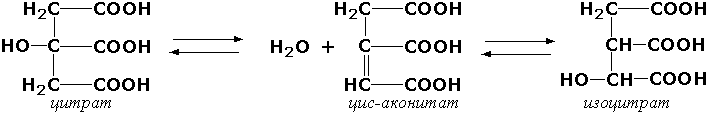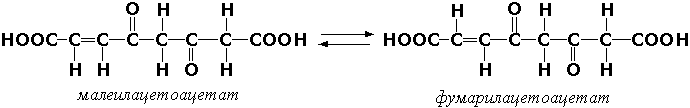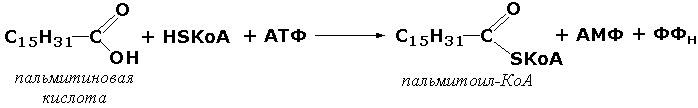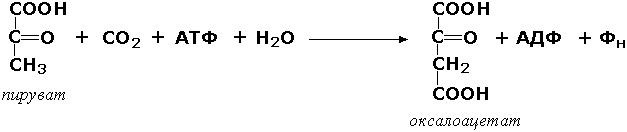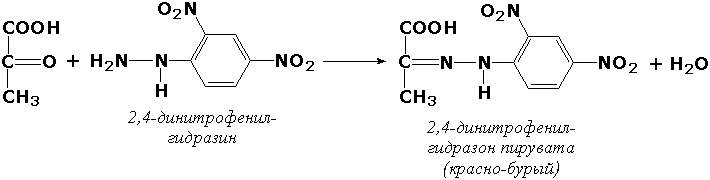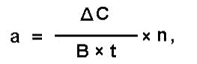ПОДПИСАТЬСЯ НА РАССЫЛКУ
Свойства и классификация ферментов.
Тема: «СВОЙСТВА И КЛАССИФИКАЦИЯ ФЕРМЕНТОВ. ВЛИЯНИЕ ТЕМПЕРАТУРЫ И рН СРЕДЫ НА АКТИВНОСТЬ ФЕРМЕНТОВ. СПЕЦИФИЧНОСТЬ ДЕЙСТВИЯ ФЕРМЕНТОВ. ОПРЕДЕЛЕНИЕ АКТИВНОСТИ ФЕРМЕНТОВ»
1. Химическая природа ферментов. Значение ферментов для жизнедеятельности организма.
2. Основные свойства ферментов. Влияние концентрации фермента и субстрата, температуры и рН среды на скорость ферментативной реакции. Олигодинамичность и обратимость действия ферментов.
3. Специфичность действия ферментов (абсолютная, относительная и стереохимическая). Примеры.
4. Важнейший признак, положенный в основу классификации ферментов. Понятие о кодовом номере фермента. Классы ферментов: оксидоредуктазы, трансферазы, гидролазы, лиазы, изомеразы, лигазы. Тип и общее уравнение катализируемых реакций, принципы формирования подклассов.
5. Номенклатура ферментов (понятие о систематическом и рабочем (рекомендуемом) названиях ферментов, их использование).
6. Определение активности ферментов. Аналитические методы, применяемые для определения активности. Единицы общей, удельной, молекулярной активности ферментов, их использование. Формула для расчёта общей активности фермента в сыворотке крови.
| Раздел 7.1 |
Химическая природа ферментов. Значение ферментов для жизнедеятельности организма. |
|
|
|
|
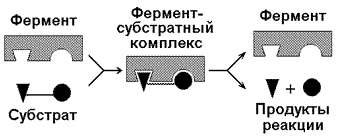
7.1.1. Протекание процессов обмена веществ в организме определяется действием многочисленных ферментов — биологических катализаторов белковой природы. Они ускоряют химические реакции и сами при этом не расходуются. Термин «фермент» происходит от латинского слова fermentum — закваска. Наряду с этим понятием в литературе используется равноценный термин «энзим» (en zyme - в дрожжах) греческого происхождения. Отсюда раздел биохимии, изучающий ферменты, получил название «энзимология». Энзимология составляет основу познания на молекулярном уровне важнейших проблем физиологии и патологии человека. Переваривание пищевых веществ и их использование для выработки энергии, образование структурных и функциональных компонентов тканей, сокращение мышц, передача электрических сигналов по нервным волокнам, восприятие света глазом, свертывание крови — каждый из этих физиологических механизмов имеет в основе каталитическое действие определенных ферментов. Было показано, что многочисленные заболевания непосредственно нарушением ферментативного катализа; определение активности ферментов в крови и других тканях даёт ценные сведения для медицинской диагностики; ферменты или их ингибиторы могут применяться как лекарственные вещества. Таким образом, знание важнейших особенностей ферментов и катализируемых ими реакций необходимо при рациональном подходе к изучению заболеваний человека, их диагностике и лечению. 7.1.2. Вещества, превращения которых катализируют ферменты, называются субстратами. Фермент, соединяясь с субстратом, образует фермент-субстратный комплекс (рисунок 7.1).
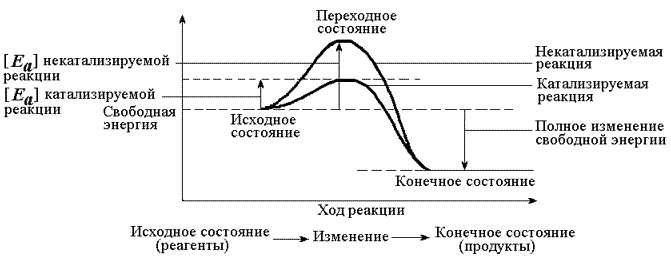
Рисунок 7.1. Образование фермент-субстратного комплекса в ходе катализируемой реакции. Образование этого комплекса способствует снижению энергетического барьера, который нужно преодолеть молекуле субстрата для вступления в реакцию (рисунок 7.2). По завершении реакции фермент-субстратный комплекс распадается на продукт (продукты) и фермент. Фермент по окончании реакции возвращается в своё исходное состояние и может взаимодействовать с новой молекулой субстрата.
Рисунок 7.2. Влияние фермента на энергетический барьер реакции. Ферменты, действуя как катализаторы, снижают энергию активации, которая требуется для того, чтобы могла произойти реакция. 7.1.3. Для ферментов характерны свойства, присущие всем белкам. В частности, молекулы ферментов, как и других белков, построены из α-аминокислот, соединённых пептидными связями. Поэтому растворы ферментов дают положительную биуретовую реакцию, а их гидролизаты - положительную нингидриновую реакцию. Нативные свойства и функции ферментов определяются наличием определённой пространственной структуры (конформации) их полипептидной цепи. Изменение этой структуры в результате тепловой денатурации приводит к потере каталитических свойств. Наличие у ферментов высокой молекулярной массы обусловливает их неспособность к диализу, а присутствие в молекулах заряженных функциональных групп - подвижность в электрическом поле. Как и другие белки, ферменты образуют коллоидные растворы, из которых могут осаждаться ацетоном, спиртом, сульфатом аммония - веществами, способствующими разрушению гидратной оболочки и нейтрализации электрического заряда. |
|
| Раздел 7.2 |
Основные свойства ферментов. Олигодинамичность и обратимость действия ферментов. Влияние концентрации фермента и субстрата, температуры и рН среды на скорость ферментативной реакции. |
|
|
|
|
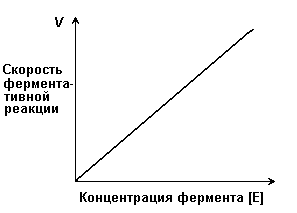
7.2.1. Белковая природа ферментов обусловливает появление у них ряда свойств, в целом нехарактерных для неорганических катализаторов: олигодинамичность, специфичность, зависимость скорости реакции от температуры, рН среды, концентрации фермента и субстрата, присутствия активаторов и ингибиторов. Под олигодинамичностью ферментов понимают высокую эффективность действия в очень малых количествах. Такая высокая эффективность объясняется тем, что молекулы ферментов в процессе своей каталитической деятельности непрерывно регенерируют. Типичная молекула фермента может регенерировать миллионы раз в минуту. Надо сказать, что и неорганические катализаторы также способны ускорять превращение такого количества веществ, которое во много раз превышает их собственную массу. Но ни один неорганический катализатор не может сравниться с ферментами по эффективности действия. Примером может служить фермент реннин, вырабатываемый слизистой оболочкой желудка жвачных животных. Одна молекула его за 10 минут при 37°С способна вызывать коагуляцию (створаживание) порядка миллиона молекул казеиногена молока. Другой пример высокой эффективности ферментов даёт каталаза. Одна молекула этого фермента при 0°С расщепляет за секунду около 50 000 молекул пероксида водорода: 2 Н2О2 Действие каталазы на пероксид водорода заключается в изменении величины энергии активации этой реакции приблизительно от 75 кДж/моль без катализатора до 21 кДж/моль в присутствии фермента. Если же в качестве катализатора этой реакции используется коллоидная платина, то энергия активации составляет всего 50 кДж/моль. 7.2.2. При изучении влияния какого-либо фактора на скорость ферментативной реакции все прочие факторы должны оставаться неизменными и по возможности иметь оптимальное значение. Мерой скорости ферментативных реакций служит количество субстрата, подвергшегося превращению в единицу времени, или количество образовавшегося продукта. Изменение скорости проводят на начальной стадии реакции, когда продукт ещё практически отсутствует, и обратная реакция не идёт. Кроме того, на начальной стадии реакции концентрация субстрата соответствует его исходному количеству. 7.2.3. Зависимость скорости ферментативной реакции (V) от концентрации фермента [Е] (рисунок 7.3). При высокой концентрации субстрата (многократно превышающей концентрацию фермента) и при постоянстве других факторовскорость ферментативной реакции пропорциональна концентрации фермента. Поэтому зная скорость реакции, катализируемой ферментом, можно сделать вывод о его количестве в исследуемом материале.
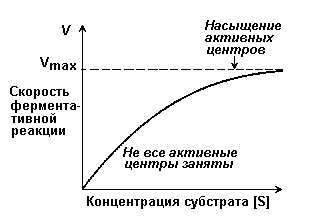
Рисунок 7.3. Зависимость скорости ферментативной реакции от концентрации фермента 7.2.4. Зависимость скорости реакции от концентрации субстрата [S]. График зависимости имеет вид гиперболы (рисунок 7.4). При постоянной концентрации фермента скорость катализируемой реакции возрастает с увеличением концентрации субстрата до максимальной величины Vmax, после чего остаётся постоянной. Это следует объяснить тем, что при высоких концентрациях субстрата все активные центры молекул фермента оказываются связанными с молекулами субстрата. Любое избыточное количество субстрата может соединиться с ферментом лишь после того, как образуется продукт реакции и освободится активный центр.
Рисунок 7.4. Зависимость скорости ферментативной реакции от концентрации субстрата. Зависимость скорости реакции от концентрации субстрата может быть выражена уравнением Михаэлиса — Ментен:
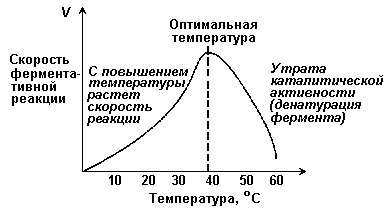
где V — скорость реакции при концентрации субстрата [S] , Vmax —максимальная скорость и KM —константа Михаэлиса. Константа Михаэлиса равна концентрации субстрата, при которой скорость реакции составляет половину максимальной. Определение KM и Vmax имеет важное практическое значение, так как позволяет количественно описать большинство ферментативных реакций, включая реакции с участием двух и более субстратов. Различные химические вещества, изменяющие активность ферментов, по-разному воздействуют на величины Vmax и KM. 7.2.5. Зависимость скорости реакции от t – температуры, при которой протекает реакция (рисунок 7.5), имеет сложный характер. Значение температуры, при котором скорость реакции максимальна, представляет собой температурный оптимум фермента. Температурный оптимум большинства ферментов организма человека приблизительно равен 40°С. Для большинства ферментов оптимальная температура равна или выше тойц температуры, при которой находятся клетки.
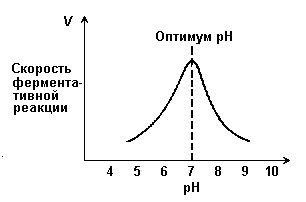
Рисунок 7.5. Зависимость скорости ферментативной реакции от температуры. При более низких температурах (0° — 40°С) скорость реакции увеличивается с ростом температуры. При повышении температуры на 10°С скорость ферментативной реакции удваивается (температурный коэффициент Q10 равен 2). Повышение скорости реакции объясняется увеличением кинетической энергии молекул. При дальнейшем повышении температуры происходит разрыв связей, поддерживающих вторичную и третичную структуру фермента, то есть тепловая денатурация. Это сопровождается постепенной потерей каталитической активности. 7.2.6. Зависимость скорости реакции от рН среды (рисунок 7.6). При постоянной температуре фермент работает наиболее эффективно в узком интервале рН. Значение рН, при котором скорость реакции максимальна, представляет собой оптимум рН фермента. У большинства ферментов организма человека оптимум рН находится в пределах рН 6 – 8, но есть ферменты, которые активны при значениях рН, лежащих за пределами этого интервала (например, пепсин, наиболее активный при рН 1,5 - 2,5). Изменение рН как в кислую, так и в щелочную сторону от оптимума приводит к изменению степени ионизации кислых и основных групп аминокислот, входящих в состав фермента (например, СООН-группы аспартата и глутамата, NН2-группы лизина и т.д.). Это вызывает изменение конформации фермента, в результате чего изменяется пространственная структура активного центра и снижение его сродства к субстрату. Кроме того, при экстремальных значениях рН происходит денатурация фермента и его инактивация.
Рисунок 7.6. Зависимость скорости ферментативной реакции от рН среды. Следует отметить, что свойственный ферменту оптимум рН не всегда совпадает с рН его непосредственного внутриклеточного окружения. Это позволяет предположить, что среда, в которой находится фермент, в какой-то мере регулирует его активность. 7.2.7. Зависимость скорости реакции от присутствия активаторов и ингибиторов. Активаторы повышают скорость ферментативной реакции. Ингибиторы понижают скорость ферментативной реакции. В качестве активаторов ферментов могут выступать неорганические ионы. Предполагают, что эти ионы заставляют молекулы фермента или субстрата принять конформацию, способствующую образованию фермент-субстратного комплекса. Тем самым увеличивается вероятность взаимодействия фермента и субстрата, а следовательно и скорость реакции, катализируемой ферментом. Так, например, активность амилазы слюны повышается в присутствии хлорид-ионов. |
|
| Раздел 7.3 |
Специфичность действия ферментов (абсолютная, относительная и стереохимическая). |
|
|
|
|
7.3.1. Важным свойством, отличающим ферменты от неорганических катализаторов, является специфичность действия. Как известно, структура активного центра фермента комплементарна структуре его субстрата. Поэтому фермент из всех имеющихся в клетке веществ выбирает и присоединяет только свой субстрат. Для ферментов характерна специфичность не только по отношению к субстрату, но и в отношении пути превращения субстрата. У ферментов различают абсолютную, относительную и стереохимическую специфичность. 7.3.2. Абсолютная специфичность – избирательная способность фермента катализировать только единственное из возможных превращений одного субстрата. Это можно объяснить конформационной и электростатической комплементарностью молекул субстрата и фермента. Например, фермент аргиназа катализирует только гидролиз аминокислоты аргинина, фермент уреаза – только расщепление мочевины и не действуют на другие субстраты. 7.3.3. Относительная специфичность – избирательная способность фермента катализировать однотипные превращения сходных по строению субстратов. Такие ферменты оказывают воздействие на одинаковые функциональные группы или на один и тот же тип связей в молекулах субстратов. Так, например, разные гидролитические ферменты действуют на определённый тип связей:
Действие этих ферментов распространяется на большое число субстратов, что позволяет организму обойтись малым количеством пищеварительных ферментов - иначе их потребовалось бы намного больше. 7.3.4. Стереохимическая (оптическая) специфичность - избирательная способность фермента катализировать превращение только одного из возможных пространственных изомеров субстрата. Так, большинство ферментов млекопитающих катализирует превращение толькл L-изомеров аминокислот, но не D-изомеров. ферменты, участвующие в обмене моносахаридов, наоборот, катализируют превращение только D-, но не L-фосфосахаров. Гликозидазы специфичны не только к моносахаридному фрагменту, но и характеру гликозидной связи. Например, α-амилаза расщепляет α–1,4-гликозидные связи в молекуле крахмала, но не действует на α–1,2-гликозидные связи в молекуле сахарозы. |
|
| Раздел 7.4 |
Основные принципы, положенные в основу современной классификации и номенклатуры ферментов. |
|
7.4.1. В настоящее время известно более двух тысяч химических реакций, катализируемых ферментами, и число это непрерывно возрастает. Чтобы ориентироваться в таком множестве превращений. возникла настоятельная необходимость в систематизированной классификации и номенклатуре, при помощи которой любой фермент можно было бы точно идентифицировать. Номенклатура, которой пользовались до середины XX века, была весьма далека от совершенства. Исследователи, открывая новый фермент, давали ему название по своему усмотрению, что неизбежно вело к путанице и всевозможным противоречиям. Некоторые названия оказались ошибочными, другие ничего не говорили о природе катализируемой реакции. Учёные разных школ часто употребляли разные названия для одного и того же фермента или, наоборот, одно и то же название для нескольких разных ферментов. Было решено разработать рациональную международную классификацию и номенклатуру ферментов, которой могли бы пользоваться биохимики всех стран. С этой целью при Международном союзе биохимии и молекулярной биологии (International Union of Biochemistry and Molecular Biology, IUВMB) была создана Комиссия по ферментам, предложившая в 1964 году основные принципы такой классификации и номенклатуры. Она постоянно совершенствуется и дополняется, в настоящее время действует уже шестая редакция этой номенклатуры (1992 год), к которой ежегодно выходят дополнения. |
|
7.4.2. В основу классификации положен важнейший признак, по которому один фермент отличается от другого — это катализируемая им реакция. Число типов химических реакций сравнительно невелико, что позволило разделить все известные в настоящее время ферменты на 6 важнейших классов, в зависимости от типа катализируемой реакции. Такими классами являются:
- оксидоредуктазы (окислительно-восстановительные реакции);
- трансферазы (перенос функциональных групп);
- гидролазы (реакции расщепления с участием воды);
- лиазы (разрыв связей без участия воды);
- изомеразы (изомерные превращения);
- лигазы (синтез с затратой молекул АТФ).
7.4.3. Ферменты каждого класса делят на подклассы, руководствуясь строением субстратов. В подклассы объединяют ферменты, действующие на сходно построенные субстраты. Подклассы разбивают на подподклассы, в которых ещё строже уточняют структуру химических групп, отличающих субстраты друг от друга. Внутри подподклассов перечисляют индивидуальные ферменты. Все подразделения классификации имеют свои номера. Таким образом, любой фермент получает свой уникальный кодовый номер, состоящий из четырёх чисел, разделённых точками. Первое число обозначает класс, второе - подкласс, третье - подподкласс, четвёртое - номер фермента в пределах подподкласса. Например, фермент α-амилаза, расщепляющая крахмал, обозначается как 3.2.1.1, где:
3 — тип реакции (гидролиз);
2 — тип связи в субстрате (гликозидная);
1 — разновидность связи (О-гликозидная);
1 — номер фермента в подподклассе
Вышеописанный десятичный способ нумерации имеет одно важное преимущество: он позволяет обойти главное неудобство сквозной нумерации ферментов, а именно: необходимость при включении в список вновь открытого фермента изменять номера всех последующих. Новый фермент может быть помещён в конце соответствующего подподкласса без нарушения всей остальной нумерации. Точно так же при выделении новых классов, подклассов и подподклассов их можно добавлять без нарушения порядка нумерации ранее установленных подразделений. Если после получения новой информации возникает необходимость изменить номера некоторым ферментам, прежние номера не присваивают новым ферментам, чтобы избежать недоразумений.
Говоря о классификации ферментов, следует также отметить, что ферменты классифицируются не как индивидуальные вещества, а как катализаторы определённых химических превращений. Ферменты, выделенные из разных биологических источников и катализирующие идентичные реакции, могут существенно отличаться по своей первичной структуре. Тем не менее в классификационном списке все они фигурируют под одним и тем же кодовым номером.
Итак, знание кодового номера фермента позволяет:
- устранить неоднозначности, если разные исследователи используют одно и то же название для различных ферментов;
- сделать поиск информации в литературных базах данных более эффективным;
- получить в других базах данных дополнительную информацию о последовательности аминокислот, пространственной структуре фермента, генах, кодирующих ферментные белки.
аздел 7.5
Понятие о систематическом и рабочем названии фермента, их использование.
7.5.1. Система классификации, разработанная Комиссией по ферментам, включает также и вновь созданную номенклатуру ферментов, которая строится по специальным принципам. Согласно рекомендациям IUBMB, ферменты получают два рода названий: систематическое и рабочее (рекомендуемое).
7.5.2. Систематическое название составляется из двух частей. Первая часть содержит название субстрата или субстратов, часто — наименование кофермента, вторая часть указывает на природу катализируемой реакции и включает название класса, к которому относится данный фермент. При необходимости приводится дополнительная информация о реакции в скобках после второй части названия. Систематическое название присваивается только тем ферментам, каталитическое действие которых полностью изучено.
Например, систематическое название α-амилазы — 1,4-α-D-глюкан-глюканогидролаза. Конечно, такое название очень неудобно для запоминания и произнесения. Поэтому наряду с систематическими Комиссия по ферментам IUBMB даёт рекомендует использовать рабочие (упрощённые) названия ферментов.
7.5.3. Рабочее название фермента должно быть достаточно коротким для употребления. В качестве рабочего названия в ряде случаев может быть использовано тривиальное название, если оно не является ошибочным или двусмысленным. В других случаях оно строится на тех же общих принципах, что и систематическое название, но с минимальной детализацией. Конкретные примеры систематических и рабочих названий ферментов приводятся в следующем разделе данной темы курса. В научных публикациях при первом упоминании о ферменте принято указывать его систематическое название и кодовый номер, а в дальнейшем пользоваться его рабочим названием.
7.5.4. Основные правила построения систематических и рабочих названий разных классов ферментов:
Оксидоредуктазы
 Систематическое название ферментов этого класса строится по схеме донор: акцептор - оксидоредуктаза.Согласно тривиальной номенклатуре, оксидоредуктазы, отщепляющие атомы водорода или электроны и переносящие их на любой акцептор, кроме кислорода, называются дегидрогеназами. Оксидоредуктазы, использующие кислород в качестве акцептора атомов водорода или электронов, называются оксидазами.Некоторые ферменты, которым свойственно преимущественно восстанавливающее действие, носят названиередуктаз. Все перечисленные наименования могут быть использованы для построения рабочего названияоксидоредуктаз.
Систематическое название ферментов этого класса строится по схеме донор: акцептор - оксидоредуктаза.Согласно тривиальной номенклатуре, оксидоредуктазы, отщепляющие атомы водорода или электроны и переносящие их на любой акцептор, кроме кислорода, называются дегидрогеназами. Оксидоредуктазы, использующие кислород в качестве акцептора атомов водорода или электронов, называются оксидазами.Некоторые ферменты, которым свойственно преимущественно восстанавливающее действие, носят названиередуктаз. Все перечисленные наименования могут быть использованы для построения рабочего названияоксидоредуктаз.
Трансферазы
 Систематическое название ферментов, ускоряющих такие реакции, составляют по форме донор:акцептор (транспортируемая группа) трансфераза. В рабочем названии обычно указывается только один специфический субстрат или продукт наряду с названием транспортируемой группировки.
Систематическое название ферментов, ускоряющих такие реакции, составляют по форме донор:акцептор (транспортируемая группа) трансфераза. В рабочем названии обычно указывается только один специфический субстрат или продукт наряду с названием транспортируемой группировки.
Гидролазы
 Систематическое название составляется по форме субстрат-гидролаза. У гидролаз, специфически отщепляющих определённую группу, эта группа может быть указана в виде префикса. Рабочее название чаще всего составляется из названия гидролизуемого субстрата с добавлением окончания -аза. Следует, однако, отметить, что вследствие достаточно сложного и зачастую до конца не выявленного характера специфичности многих гидролаз не всегда удаётся дать им систематическое название. В этих случаях рекомендовано использовать эмпирические названия, присвоенные им при первом описании. Так, не имеют систематического названия такие ферменты, как пепсин, папаин, тромбин.
Систематическое название составляется по форме субстрат-гидролаза. У гидролаз, специфически отщепляющих определённую группу, эта группа может быть указана в виде префикса. Рабочее название чаще всего составляется из названия гидролизуемого субстрата с добавлением окончания -аза. Следует, однако, отметить, что вследствие достаточно сложного и зачастую до конца не выявленного характера специфичности многих гидролаз не всегда удаётся дать им систематическое название. В этих случаях рекомендовано использовать эмпирические названия, присвоенные им при первом описании. Так, не имеют систематического названия такие ферменты, как пепсин, папаин, тромбин.
Лиазы
 Систематическое название ферментов строится по схеме: субстрат-отщепляемая группа-лиаза. Чтобы уточнить, какая группа отщепляется, используются префиксы "карбокси-", "аммиак", "гидро-" и т.д. В качестве рабочих названий ферментов сохраняются тривиальные названия типа "декарбоксилаза", "альдолаза", "дегидратаза", "десульфгидраза". Лиазы делятся на подклассы в зависимости от характера разрываемых связей
Систематическое название ферментов строится по схеме: субстрат-отщепляемая группа-лиаза. Чтобы уточнить, какая группа отщепляется, используются префиксы "карбокси-", "аммиак", "гидро-" и т.д. В качестве рабочих названий ферментов сохраняются тривиальные названия типа "декарбоксилаза", "альдолаза", "дегидратаза", "десульфгидраза". Лиазы делятся на подклассы в зависимости от характера разрываемых связей
Изомеразы
Систематическое название ферментов включает название субстрата и слово изомераза, которому предшествует указание типа реакции изомеризации. Рабочие названия подобны (с некоторыми упрощениями) систематическим названиям.
Лигазы
 Систематическое название образуется из названий соединяемых субстратов в сочетании со словомлигаза. В скобках указывается продукт, образующийся в результате гидролиза нуклеозидтрифосфата (например, АДФ или АМФ). Рабочее название ферментов этого класса составляется, как правило, из названия продукта реакции в сочетании со словом синтетаза.
Систематическое название образуется из названий соединяемых субстратов в сочетании со словомлигаза. В скобках указывается продукт, образующийся в результате гидролиза нуклеозидтрифосфата (например, АДФ или АМФ). Рабочее название ферментов этого класса составляется, как правило, из названия продукта реакции в сочетании со словом синтетаза.
| Раздел 7.6.1 |
ОКСИДОРЕДУКТАЗЫ. |
|
|
|
|
К классу оксидоредуктаз относят ферменты, катализирующие окислительно-восстановительные реакции. Общая схема их может быть представлена следующим образом: AH2+B где AH2 —донор водорода, B — акцептор водорода. В живых организмах окисление осуществляется преимущественно путём отщепления атомов водорода или электронов от субстратов-доноров. Акцепторами атомов водорода или электронов могут быть различные вещества - коферменты (НАД, НАДФ, ФАД, ФМН, глутатион, липоевая кислота, убихинон), цитохромы. железосерные белки и кислород. Подклассы оксидоредуктаз формируются в зависимости от природы функциональной группы донора водорода (электронов). Всего выделяют 19 подклассов. Основными из них являются следующие: Оксидоредуктазы, действующие на СН-ОН-группу доноров. Ферменты, относящиеся к этому подклассу, окисляют спиртовые группы до альдегидных или кетонных групп. В качестве примера можно привести фермент алкогольдегидрогеназу (алкоголь:НАД-оксидоредуктаза; КФ 1.1.1.1). участвующую в метаболизме этанола в тканях:
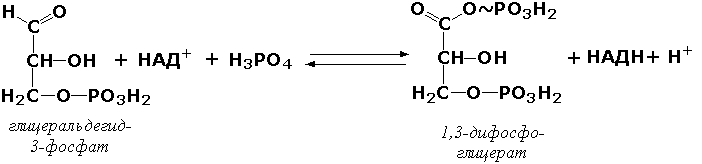
Кроме окисления спиртов, ферменты этого подкласса участвуют в дегидрировании оксикислот (молочной, яблочной, изолимонной), моносахаридов и других соединений, содержащих гидроксильные группы. Оксидоредуктазы, действующие на альдегидную или кетонную группу доноров. Эти ферменты окисляют альдегиды и кетоны до карбоновых кислот. К примеру, представитель данного подкласса - глицеральдегид-3-фосфатдегидрогеназа (D-глицеральдегид-3-фосфат:НАД-оксидоредуктаза (фосфорилирующая), КФ 1.2.1.12) - катализирует одну из промежуточных реакций распада глюкозы:
Важно отметить, что продукт этой реакции содержит богатую энергией фосфатную связь в 1-ом положении. Остаток фосфорной кислоты, образующий эту связь, может быть перенесён от 1,3-дифосфоглицерата на АДФ с образованием АТФ (см. далее). Оксидоредуктазы, действующие на СН-СН-группу доноров. В результате катализируемых ими реакций СН-СН-группы превращаются в С=С-группы. то есть происходит образование ненасыщенных соединений из насыщенных. Например, фермент цикла трикарбоновых кислот сукцинатдегидрогеназа (сукцинат:акцептор - оксидоредуктаза, КФ 1.3.99.1) ускоряет окисление янтарной кислоты с образованием ненасыщенной фумаровой кислоты:
Оксидоредуктазы, действующие на CH-NH2-группу доноров. Эти ферменты катализируют окислительное дезаминирование аминокислот и биогенных аминов. Амины при этом превращаются в альдегиды или кетоны, аминокислоты - в кетокислоты и выделяется аммиак. Так, глутаматдегидрогеназа (L-глутамат:НАД(Ф) - оксидоредуктаза (дезаминирующая), КФ 1.4.1.3) принимает участие в следующем превращении глутамата:
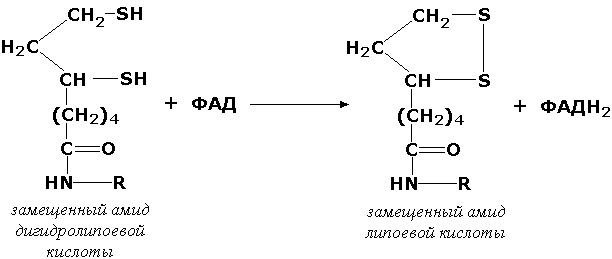
Оксидоредуктазы, действующие на серосодержащие группы доноров, катализируют окисление тиоловых (сульфгидрильных) групп до дисульфидных, а сульфитов - до сульфатов. Примером фермента является дигидролипоилдегидрогеназа (КФ 1.8.1.4), катализирующая одну из промежуточных реакций окислительного декарбоксилирования пирувата:
Оксидоредуктазы, действующие на пероксид водорода в качестве акцептора, сравнительно немногочисленны и объединены в отдельный подкласс, известный также под тривиальным названием пероксидазы. Примером фермента является глутатионпероксидаза (глутатион:Н2О2 - оксидоредуктаза. КФ 1.11.1.9), участвующая в инактивации пероксида водорода в эритроцитах, печени и некоторых других тканях:
Оксидоредуктазы, действующие на пару доноров с включением молекулярного кислорода, или монооксигеназы - ферменты, катализирующие окисление органических соединений молекулярным кислородом, приводящее к включению одного из атомов кислорода в молекулы этих соединений. При этом второй атом кислорода включается в молекулу воды. Так реакция превращения фенилаланина в тирозин катализируется фенилаланин-4-монооксигеназой (КФ 1.14.16.1):
У некоторых людей генетический дефект этого фермента служит причиной заболевания, которое носит название фенилкетонурии. К монооксигеназам относится также фермент, известный под названием цитохром Р450 (КФ 1.14.14.1) Он содержится, главным образом, в клетках печени и осуществляет гидроксилирование чуждых организму липофильных соединений, образующихся в качестве побочных продуктов реакций или попадающих в организм извне. Например, индол, образующийся из триптофана в результате деятельности микроорганизмов кишечника, подвергается в печени гидроксилированию по следующей схеме:
Появление гидроксильной группы повышает гидрофильность веществ и облегчает их последующий вывод из организма. Кроме того, цитохром Р450 принимает участие в отдельных этапах превращения холестерина и стероидных гормонов. Наличие у живых организмов высокоэффективной системы цитохрома Р450 приводит в ряде случаев к нежелательным практическим следствиям: сокращает время пребывания в организме человека лекарственных препаратов и тем самым снижает их терапевтический эффект. Оксидоредуктазы, действующие на один донор с включением молекулярного кислорода, или диоксигеназы, катализируют превращения, в ходе которых оба атома молекулы О2включаются в состав окисляемого субстрата. Например, в процессе катаболизма фенилаланина и тирозина происходит образование из гомогентизиновой кислоты малеилацетоацетата, в состав которого включаются оба атома кислорода:
Фермент, катализирующий эту реакцию, называется гомогентизат-1,2-диоксигеназой (КФ 1.13.11.5). В ряде случаев встречается врождённый дефицит этого фермента, что приводит к развитию заболевания, называемого алкаптонурией. |
|
| Раздел 7.6.2 |
ТРАНСФЕРАЗЫ. |
|
|
|
| Трансферазы - класс ферментов, катализирующих перенос функциональных групп от одного соединения к другому. В общем виде эти превращения можно записать:
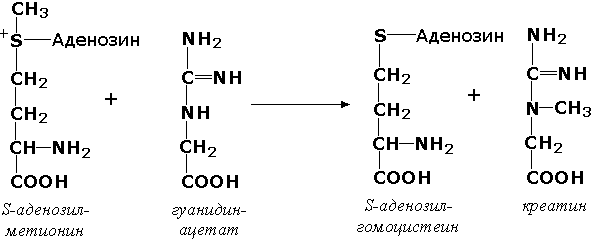
где Х - переносимая функциональная группа. AX - донор группировки, В - акцептор. Подразделение на подклассы зависит от природы переносимых группировок. Трансферазы, переносящие одноуглеродные фрагменты. К этому подклассу относятся ферменты, ускоряющие перенос метильных (—CH3), метиленовых (—СН2—), метенильных (—СН=), формильных и родственных им групп. Так, при участии гуанидинацетат-метилтрансферазы (S-аденозилметионингуанидинацетат-метилтрансфераза, КФ 2.1.1.2) происходит синтез биологически активного вещества креатина:
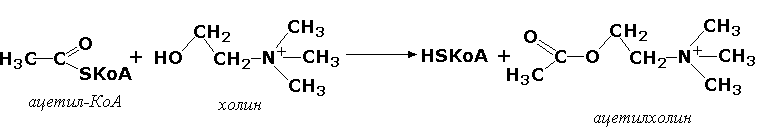
Трансферазы, переносящие остатки карбоновых кислот (ацилтрансферазы). Они катализируют разнообразные химические процессы связанные с переносом остатков различных кислот (уксусной, пальмитиновой и др.) преимущественно от тиоэфиров коэнзима А на различные акцепторы. Примером реакции трансацетилирования может быть образование медиатора ацетилхолина при участии холин-ацетилтрансферазы (ацетил-КоА:холин-О-ацетилтрансфераза, КФ 2.3.1.6):
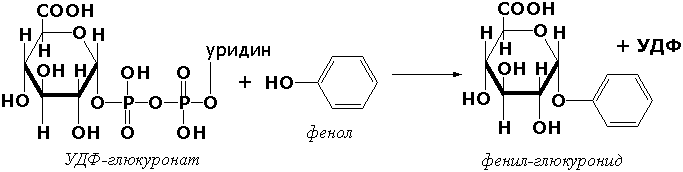
Трансферазы, переносящие гликозильные остатки (гликозилтрансфсразы), катализируют транспорт гликозильных остатков из молекул фосфорных эфиров к молекулам моносахаридов, полисахаридов и других веществ. Эти ферменты, в частности, играют основную роль в синтезе гликогена и крахмала, а также в первой фазе их деструкции. Ещё один фермент этого подкласса - УДФ-глюкуронилтрансфераза (УДФ-глюкуронат-глюкуронил-трансфераза (неспецифичная к акцептору), КФ 2.4.1.17) - участвует в процессах обезвреживания эндогенных и чужеродных токсических веществ в печени:
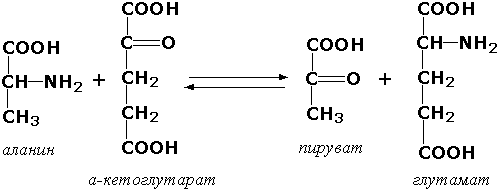
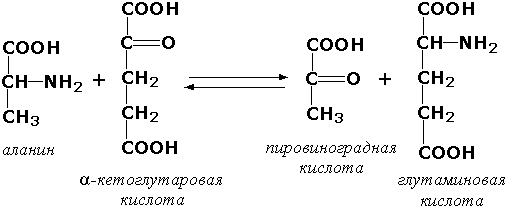
Трансферазы, переносящие азотистые группы. В этот подкласс входят аминотрансферазы, ускоряющие перенос α-аминогруппы аминокислот к α-углеродному атому кетокислот. Наиболее важным из этих ферментов является аланинаминотрансфераза (L-аланин:2-оксоглутарат-аминотрансфераза, КФ 2.6.1.2). катализирующая реакцию:
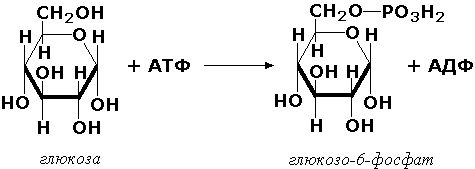
Трансферазы, переносящие фосфатные группы (фосфотрансферазы). Эта группа ферментов катализирует биохимические процессы, связанные с транспортом остатков фосфорной кислоты на различные субстраты. Указанные процессы имеют важное значение для жизнедеятельности организма, так как обеспечивают превращение ряда веществ в органические фосфоэфиры, обладающие высокой химической активностью и легко вступающие в последующие реакции. Фосфотрансферазы, использующие в качестве донора фосфата АТФ, принято называть киназами. Широко распространённым ферментом является гексокиназа (ATФ:D-гексоза-6-фосфотрансфераза. КФ 2.7.1.1.), ускоряющая перенос фосфатной группы с АТФ на моносахариды:
В некоторых случаях возможен и обратный перенос фосфатной группы с субстрата на АДФ с образованием АТФ. Так, фермент фосфоглицераткиназа (АТФ:D-3-фосфоглицерат-1-фосфотрансфераза, КФ 2.7.2.3) осуществляет превращение упомянутого ранее (см. "Оксидоредуктазы") 1.3-дифосфоглицерата:
Подобные реакции фосфорилирования АДФ с образованием АТФ, сопряжённые с превращением субстрата (а не с переносом электронов в дыхательной цепи), получили название реакций субстратного фосфорилирования. Роль этих реакций в клетке значительно возрастает при недостатке кислорода в тканях. |
|
| Раздел 7.6.3 |
ГИДРОЛАЗЫ. |
|
|
|
|
Гидролазы - класс ферментов, катализирующих реакции расщепления органических соединений при участии воды (реакции гидролиза). Эти реакции протекают по следующей схеме:
где А-В - сложное соединение, А-Н и В-ОН - продукты его гидролиза. Реакции этого типа активно протекают в организме; они идут с выделением энергии и, как правило, необратимы. Подклассы гидролаз формируются в зависимости от типа гидролизуемой связи. Наиболее важными являются следующие подклассы: Гидролазы, действующие на сложные эфиры (или эстеразы) гидролизуют сложные эфиры карбоновой, фосфорной, серной и других кислот. Широко распространённым ферментом этого подкласса является триацилглицероллипаза (гидролаза эфиров глицерола, КФ 3.1.1.3). ускоряющая гидролиз ацилглицеролов:
Другие представители эстераз расщепляют сложноэфирные связи в ацетилхолине (ацетилхолинэстераза), фосфолипидах (фосфолипазы), нуклеиновых кислотах (нуклеазы), фосфоорганических эфирах (фосфатазы). Гидролазы, действующие на гликозидные связи (гликозидазы) ускоряют реакции гидролиза олиго- и полисахаридов, а также других соединений, содержащих моносахаридные остатки (например, нуклеозидов). Характерным представителем является сахараза (β-D-фруктофуранозид-фруктогидролаза, КФ 3.2.1.26). катализирующая расщепление сахарозы:
Гидролазы, действующие на пептидные связи (пептидазы), катализируют реакции гидролиза пептидных связей в белках и пептидах. К этой группе относятся пепсин, трипсин, химотрипсин, катепсин и другие протеолитические ферменты. Гидролиз пептидных связей происходит по следующей схеме:
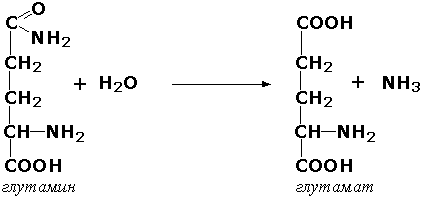
Гидролазы, действующие на C-N-связи, отличающиеся от пептидных, - ферменты, ускоряющие гидролиз амидов органических кислот. Представитель этого подкласса - глутаминаза(L-глутамил-амидогидролаза, КФ 3.5.1.2) - участвует в поддержании кислотно-основного состояния организма, катализируя в почках гидролиз глутамина:
|
|
| Раздел 7.6.4 |
ЛИАЗЫ. |
|
|
|
|
Лиазы - класс ферментов, катализирующих негидролитические реакции расщепления субстратов с образованием двойных связей или, наоборот, присоединения по месту разрыва двойной связи. Общая схема этих реакций:
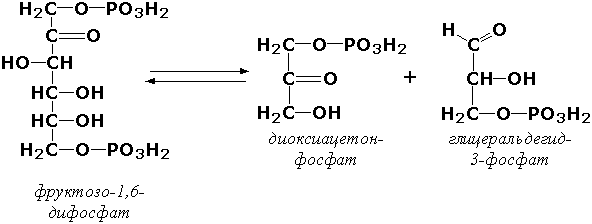
где А—В - субстрат, А и В - продукты реакции. В результате таких реакций часто выделяются простые вещества, например, СО2, NH3, H2О. Углерод-углерод-лиазы катализируют разрыв связи между двумя атомами углерода. Среди них наибольшее значение имеют карбокси-лиазы (декарбоксилазы), под влиянием которых осуществляется декарбоксилирование a-кето- и аминокислот, лиазы кетокислот , к которым относится цитратсинтаза, альдегид-лиазы (альдолазы). К последним относитсяфруктозодифосфатальдолаза (фруктозо-1,6-дифосфат-D-глицеральдегид-3-фосфат-лиаза, КФ 4.1.2.13), катализирующая реакцию:
Углерод-кислород-лиазы катализируют разрыв связи между атомами углерода и кислорода. В этот подкласс входят прежде всего гидро-лиазы, участвующие в реакциях дегидратации и гидратации. Примером может служить сериндегидратаза (L-серин-гидро-лиаза (дезаминирующая), КФ 4.2.1.3), осуществляющая превращение:
Иногда за основу рабочего названия может быть принята обратная реакция с применением термина "гидратаза". Так, для фермента цикла трикарбоновых кислот L-малат-гидро-лиазы (КФ 4.2.1.2) рекомендовано название "фумаратгидратаза":
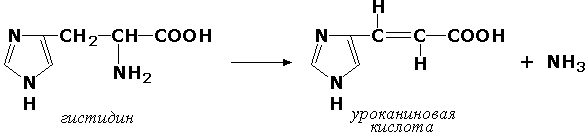
Углерод-азот-лиазы участвуют в отщеплении азотсодержащих групп. Представителем этого подкласса является гистидин-аммиак-лиаза (L-гистидин-аммиак-лиаза, КФ 4.3.1.3), участвующая в дезаминировании гистидина:
Углерод-сера-лиазы катализируют отщепление сульфгидрильных групп. К этому подклассу относятся десульфгидразы серу содержащих аминокислот, например,цистеиндесульфгидраза (L-цистеин-сероводород-лиаза (дезаминирующая), КФ 4,4.1.1). |
|
| Раздел 7.6.5 |
ИЗОМЕРАЗЫ. |
|
|
|
|
Изомеразы - класс ферментов, ускоряющих процессы внутримолекулярных превращений с образованием изомеров. Схематически реакции такого типа могут быть представлены следующим образом:
где А и А' - вещества-изомеры. Изомеразы - сравнительно немногочисленный класс ферментов, он подразделяется на следующие подклассы в зависимости от типа катализируемой реакции изомеризации: Рацемазы и эпимеразы катализируют взаимопревращение изомеров, содержащих асимметрические атомы углерода. Рацемазами называются ферменты, действующие на субстраты с одним асимметрическим атомом, например, превращающие L-аминокислоты в D-аминокислоты. Одним из таких ферментов является aлaнинрацемаза (аланин-рацемаза. КФ 5.1.1.1), катализирующая реакцию:
Эпимеразами называются ферменты, действующие на субстраты с несколькими асимметрическими атомами углерода. К таким ферментам относится УДФ-глюкозо-эпимераза (УДФ-глюкоза-4-эпимераза, КФ 5.1.3.2). участвующая в процессах взаимопревращения моносахаридов:
Цис-транс-изомеразы - ферменты, вызывающие изменение геометрической конфигурации относительно двойной связи. Примером такого фермента являетсямалеилацетоацетатизомераза (малеилацетоацетат-цис-транс-изомераза, КФ 5.2.1.2), участвующая в катаболизме фенилаланина и тирозина и переводящая малеилацетоацетат (см. 4.6.1) в фумарилацетоацетат:
Внутримолекулярные оксидоредуктазы - изомеразы, катализирующие взаимопревращения альдоз и кетоз. При этом происходит окисление СН-ОН-группы с одновременным восстановлением соседней С=О-группы. Так, триозофосфатизомераза (D-глицеральдегид-3-фосфат-кетол-изомераза, КФ 5.3.1.1) катализирует одну из реакций углеводного обмена:
К изомеразам относятся также внутримолекулярные трансферазы, осуществляющие перенос одной группы с одной части молекулы субстрата на другую часть той же молекулы, ивнутримолекулярные лиазы, катализирующие реакции дециклизации, а также превращения одного типа кольца в другой. Следует подчеркнуть, что не все биохимические процессы. результатом которых является изомеризация, катализируются изомеразами. Так, изомеризация лимонной кислоты в изопимонную происходит при участии фермента аконитатгидратазы (цитрат (изоцитрат)-гидро-лиаза, КФ 4.2.1.3), катализирующей реакции дегидратации-гидратации с промежуточным образованием цис-аконитовой кислоты:
|
|
| Раздел 7.6.6 |
ЛИГАЗЫ. |
|
|
|
|
Лигазы - класс ферментов, катализирующих синтез органических соединений из активированных за счет распада АТФ (или ГТФ, УТФ, ЦТФ) исходных веществ. Для ферментов этого класса сохраняется также тривиальное название синтетазы. В связи с этим, согласно рекомендациям IUBMB, термин "синтетазы" не должен применяться для ферментов, в действии которых не участвуют нуклеозидтрифосфаты. Реакции, катализируемые лигазами (синтетазами), протекают по схеме:
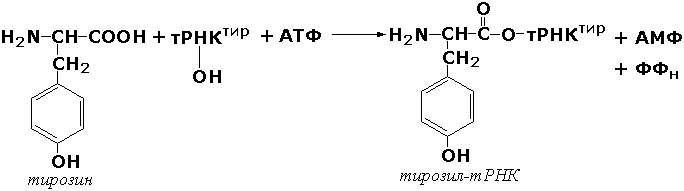
где А и В - взаимодействующие вещества; А—В - вещество, образующееся в результате взаимодействия. Поскольку в результате действия этих ферментов образуются новые химические связи, подклассы VI класса формируются в зависимости от характера вновь образованных связей. Лигазы, образующие связи углерод-кислород. К ним относится группа ферментов, известных как аминокислота-тРНК-лигазы (аминоацил-тРНК-синтетазы). которые катализируют реакции взаимодействия аминокислот и соответствующих транспортных РНК. В этих реакциях образуются активные формы аминокислот, способные участвовать в процессе синтеза белка на рибосомах. Примером фермента может служить тирозил-тРНК-синтетаза (L-тирозин:тРНК-лигаза (АМФ-образующая), КФ 6.1.1.1), участвующая в реакции:
Лигазы, образующие связи углерод-сера. Этот подкласс представлен в первую очередь ферментами, катализирующими образование тиоэфиров жирных кислот с коэнзимом А. При участии этих ферментов синтезируются ацил-КоА - активные формы жирных кислот, способные вступать в различные реакции биосинтеза и распада. Рассмотрим одну из реакций активации жирных кислот, протекающую в присутствии фермента ацил-КоА-синтетазы (карбоновая кислота:коэнзим А-лигаза (АМФ-образующая). КФ 6.2.1.2):
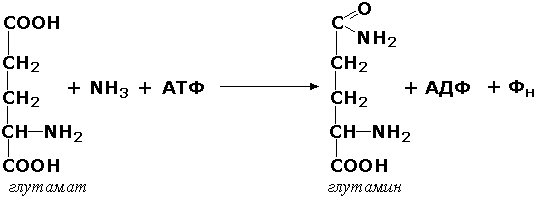
Лигазы, образующие связи углерод-азот, катализируют многочисленные реакции введения азотсодержащих групп в органические соединения. Примером может служитьглутаминсинтетаза (L-глутамин:аммиак-γ-лигаза (АДФ-образующая), КФ 6.3.1.2). участвующая в обезвреживании токсичного продукта обмена - аммиака - в реакции с глутаминовой кислотой:
Лигазы, образующие связи углерод-углерод. Из этих ферментов наиболее изучены карбоксилазы, обеспечивающие карбоксилирование ряда соединений, в результате чего происходит удлиннение углеродных цепей. Важнейшим представителем данного класса является пируваткарбоксилаза (пируват:СО2-лигаза (АДФ-образующая), КФ 6.4.1.1), ускоряющая реакцию образования оксалоацетата - ключевого соединения цикла трикарбоновых кислот и биосинтеза углеводов:
Напомним, что реакции с участием АТФ катализируются не только ферментами VI класса, но и некоторыми ферментами II класса (фосфотрансферазами или киназами). Важно уметь отличать эти типы реакций. Их различие заключается в том, что в трансферазных реакциях АТФ является донором фосфатных групп, поэтому в результате этих реакцию не происходит выделения Н3РО4 (примеры см. выше). Наоборот, в синтетазных реакциях АТФ служит источником энергии, выделяемой при её гидролизе, поэтому одним из продуктов такой реакции будет являться неорганический орто- или пирофосфат. |
|
| Раздел 7.7 |
Определение активности ферментов в биологическом материале. |
| Раздел 7.7.1 |
Правила работы с ферментами |
|
|
|
|
Ферменты, как все белки, являются относительно неустойчивыми веществами. Они легко подвергаются денатурации и инактивации. Поэтому при работе с ними необходимо выполнять определенные условия.
Для широкого внедрения различных биохимических (ферментативных) реакций вводится автоматизация наиболее общепризнанных и необходимых анализов, а также унификация и стандартизация лабораторных тестов. Это рационально и необходимо как для повышения точности, качества проведения проб, так и для сравнения данных, которые получены в разных лабораториях. Общепринятым является и обязательное параллельное исследование, наряду с изучаемой патологией, физиологического контроля — группы практически здоровых для установления нормальных, физиологических колебаний. Понимая относительность понятия «нормальная величина», следует принять, что для выявления различий в патологии и оценки патологического признака, за «норму», как правило, принимается средняя арифметическая М±1σ или 2σ (при нормальном Гауссовом распределении) в зависимости от степени колебания показателя. |
|
| Раздел 7.7.2 |
Принципы определения активности ферментов в биологическом материале. |
|
|
|
|
5.6.2. Уникальное свойство ферментов ускорять химические реакции может быть использовано для количественного определения содержания этих биокатализаторов в биологическом материале (тканевом экстракте, сыворотке крови и т.д.). При правильно подобранных экспериментальных условиях почти всегда существует пропорциональность между количеством фермента и скоростью катализируемой реакции, поэтому по активности фермента можно судить о количественном содержании его в исследуемой пробе. Измерение ферментативной активности основывается на сравнении скорости химической реакции в присутствии активного биокатализатора со скоростью реакции в контрольном растворе, в котором фермент отсутствует или инактивирован. Исследуемый материал помещают в инкубационную среду, где созданы оптимальные температура, рН среды, концентрации активаторов и субстратов. Одновременно осуществляют постановку контрольной пробы, в которую фермент не добавляют. Спустя некоторое время реакцию останавливают путём добавления различных реагентов (изменяющих рН среды, вызывающих денатурацию белков и т.д.) и проводят анализ проб. Для того чтобы определить скорость ферментативной реакции, необходимо знать:
Наиболее часто активность фермента оценивают по количеству образовавшегося продукта реакции. Так поступают, например, при определении активности аланинаминотрансферазы, катализирующей следующую реакцию:
Определяя содержание одного из продуктов реакции – пировиноградной кислоты – в пробе после инкубации и вычитая из этого значения количество пировиноградной кислоты в контрольной пробе (в неё исследуемый материал добавляется после инкубации), находят количество продукта реакции, образовавшегося за время инкубации. Активность фермента можно рассчитывать также исходя из количества израсходованного субстрата. В качестве примера можно привести способ определения активности α-амилазы – фермента, расщепляющего крахмал. Измерив содержание крахмала в пробе до и после инкубации и вычислив разность, находят количество субстрата, расщеплённого за время инкубации. |
|
| Раздел 7.7.3 |
Методы измерения активности ферментов |
|
|
|
|
Существует большое количество методов измерения активности ферментов, различающихся по технике исполнения, специфичности, чувствительности. Чаще всего для определения применяются фотоэлектроколориметрические методы. В основе этих методов лежат цветные реакции с одним из продуктов действия ферментов. При этом интенсивность окраски получаемых растворов (измеренная на фотоэлектроколориметре) пропорциональна количеству образовавшегося продукта. Например, в процессе реакций, катализируемых аминотрансферазами, накапливаются α-кетокислоты, которые дают с 2,4-динитрофенилгидразином соединения красно-бурого цвета:
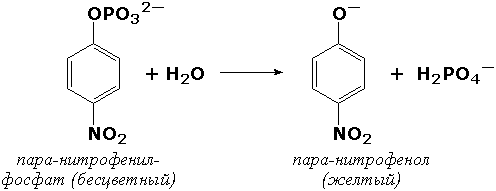
Если исследуемый биокатализатор обладает низкой специфичностью действия, то можно подобрать такой субстрат, в результате реакции с которым образуется окрашенный продукт. Примером может служить определение щелочной фосфатазы – фермента, широко распространённого в тканях человека, его активность в плазме крови существенно меняется при заболеваниях печени и костной системы. Этот фермент в щелочной среде гидролизует большую группу фосфорнокислых эфиров, как природных, так и синтетических. Одним из синтетических субстратов является паранитрофенилфосфат (бесцветный), который в щелочной среде расщепляется на ортофосфат и паранитрофенол (жёлтого цвета). За ходом реакции можно наблюдать, измеряя постепенно нарастающую интенсивность окраски раствора:
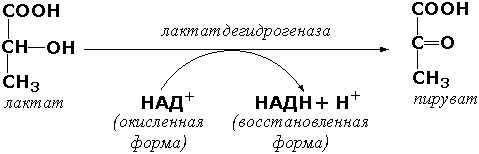
Для ферментов, обладающих высокой специфичностью действия, такой подбор субстратов, как правило, невозможен. Спектрофотометрические методы основаны на изменении ультрафиолетового спектра химических веществ, принимающих участие в реакции. Большинство соединений поглощает ультрафиолетовые лучи, причём поглощаемые длины волн характерны для присутствующих в молекулах этих веществ определённых групп атомов. Ферментативные реакции вызывают внутримолекулярные перегруппировки, в результате которых меняется ультрафиолетовый спектр. Эти изменения можно зарегистрировать на спектрофотометре. Спектрофотометрическими методами, например, определяют активность окислительно-восстановительных ферментов, содержащих в качестве коферментов НАД или НАДФ. Эти коферменты действуют как акцепторы или доноры атомов водорода и, таким образом, либо восстанавливаются, либо окисляются в процессах метаболизма. Восстановленные формы этих коферментов имеют ультрафиолетовый спектр с максимумом поглощения при 340 нм, окисленные формы этого максимума не имеют. Так, при действии лактатдегидрогеназы на молочную кислоту происходит перенос водорода на НАД, что приводит к увеличению поглощения НАДН при 340 нм. Величина этого поглощения в оптических единицах пропорциональна количеству образовавшейся восстановленной формы кофермента.
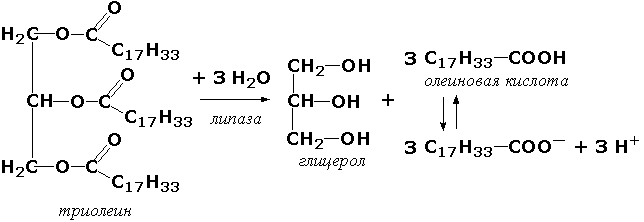
По изменению содержания восстановленной формы кофермента можно определить активность фермента. Флюориметрические методы. В основе этих методов лежит явление флюоресценции, которое заключается в том, что исследуемый объект под влиянием облучения излучает свет с более короткой длиной волны. Флюориметрические методы определения активности ферментов более чувствительны, чем спектрофотометрические. Сравнительно новыми и ещё более чувствительными являются хемилюминесцентные методы с применением люциферин-люциферазной системы. Такие методы позволяют определять скорость реакций, протекающих с образованием АТФ. При взаимодействии люциферина (карбоновой кислоты сложного строения) с АТФ образуется люцифериладенилат. Это соединение окисляется при участии фермента люциферазы, что сопровождается световой вспышкой. Измеряя интенсивность световых вспышек, удаётся определять количества АТФ порядка нескольких пикомолей (10–12 моль). Титрометрические методы. Ряд ферментативных реакций сопровождается изменением рН инкубационной смеси. Примером такого фермента является липаза поджелудочной железы. Липаза катализирует реакцию:
Образующиеся жирные кислоты могут быть оттитрованы, причём количество щёлочи, израсходованное на титрование, будет пропорционально количеству выделившихся жирных кислот и, следовательно, активности липазы. Определение активности этого фермента имеет клиническое значение. Манометрические методы основаны на измерении в закрытом реакционном сосуде объёма газа, выделившегося (или поглощённого) в ходе энзиматической реакции. С помощью таких методов были открыты и изучены реакции окислительного декарбоксилирования пировиноградной и α-кетоглутаровой кислот, протекающие с выделением СО2. В настоящее время эти методы используются редко. |
|
| Раздел 7.7.4 |
Единицы активности ферментов и их применение. |
|
|
|
|
Международная комиссия по ферментам предложила за единицу активности любого фермента принимать такое количество фермента, которое при заданных условиях катализирует превращение одного микромоля (10–6 моль) субстрата в единицу времени (1 мин, 1 час) или одного микроэквивалента затронутой группы в тех случаях, когда атакуется более одной группы в каждой молекуле субстрата (белки, полисахариды и другие). Должна быть указана температура, при которой проводится реакция. Результаты измерений активности ферментов могут быть выражены в единицах общей, удельной и молекулярной активности. За единицу общей активности фермента принимают такое количество фермента, которое катализирует превращение 1 мкмоль субстрата в единицу времени в расчёте на количество материала, взятого для исследования. Так, активность аланинаминотрансферазы в печени крыс равна 1670 мкмоль пирувата в час на 1 г ткани; активность холинэстеразы в сыворотке крови человека составляет 250 мкмоль уксусной кислоты в час на 1 мл сыворотки при 37°C. Особого внимания исследователя требуют высокие значения активности фермента как в норме, так и в патологии. Рекомендуется работать с небольшими показателями активности фермента. Для этого источник фермента берут в меньшем количестве (сыворотку разводят в несколько раз физиологическим раствором, а для ткани готовят меньший процентный гомогенат). По отношению к ферменту в таком случае создаются условия насыщения субстратом, что способствует проявлению его истинной активности. Общая активность фермента рассчитывается с помощью формулы:
где а – активность фермента (общая), ΔС – разность концентраций субстрата до и после инкубации; В – количество материала, взятого на анализ, t - время инкубации; n - разведение. Следует иметь в виду, что показатели активности ферментов сыворотки крови и мочи, исследуемых в диагностических целях, выражают в единицах общей активности. Поскольку ферменты являются белками, важно знать не только общую активность фермента в исследуемом материале, но и ферментативную активность белка, находящегося в данной пробе. За единицу удельной активности принимают такое количество фермента, которое катализирует превращение 1 мкмоль субстрата в единицу времени в расчёте на 1 мг белка пробы. Для вычисления удельной активности фермента необходимо общую активность разделить на содержание белка в пробе:
Например, содержание белка в ткани печени составляет 160 мг/г. Разделив общую активность аланинаминотрансферазы (см. выше) на это значение, получаем 10,4 мкмоль пирувата/мг белка × час. Чем хуже очищен фермент, тем больше в пробе находится посторонних балластных белков, тем ниже удельная активность. В ходе очистки количество таких белков уменьшается, и соответственно удельная активность фермента повышается. Предположим, в исходном биологическом материале, являющемся источником фермента (измельчённая печень, кашица из растительной ткани), удельная активность была равна 0,5 мкмоль/ (мг белка× мин). После дробного осаждения сульфатом аммония и гель-фильтрации через сефадекс она повысилась до 25 мкмоль/ (мг белка× мин), т.е. увеличилась в 50 раз. К оценке эффективности очистки ферментных препаратов прибегают при производстве лекарственных средств энзиматической природы. Удельную активность определяют в том случае, когда нужно сопоставить активность разных препаратов одного и того же фермента. Если требуется сравнить активность разных ферментов, рассчитывают молекулярную активность. Молекулярная активность (или число оборотов фермента) – это количество моль субстрата, подвергающееся превращению под действием 1 моль фермента в единицу времени (обычно в 1 минуту). Разным ферментам присуща неодинаковая молекулярная активность. Уменьшение числа оборотов ферментов происходит под действием неконкурентных ингибиторов. Изменяя конформацию каталитического центра фермента, эти вещества понижают сродство фермента к субстрату, что приводит к уменьшению числа молекул субстрата, реагирующих с одной молекулой фермента в единицу времени. |
|
| Примеры |
Обучающие задачи и эталоны их решения. |
|
|
|
|
1. Задачи 1. Какие ферменты называют рацемазами? 2. Расшифруйте систематическое название фермента (отдельно для каждого из элементов, выделенных разными цветами): Определите: 2. Эталоны решения 1. Рацемазы - ферменты, катализирующие взаимопревращение оптических изомеров, содержащих единственный асимметрический атом углерода (см. раздел 2.3). 2. Систематическое название фермента читается с конца. Фермент относится к классу трансфераз, катализирует реакцию переноса метильной группы на гуанидинацетат (акцептор метильной группы) с S-аденозилметионина (донор метильной группы) (см. разделы 2.2 - 2.3). 3. а) В данной реакции происходит расщепление вещества без участия молекул воды б) Негидролитическое расщепление субстрата с образованием двух продуктов катализируют ферменты, относящиеся к четвёртому классу (лиазы) в) Разрывается связь между первым и вторым углеродными атомами, что приводит к отщеплению карбоксильной группы в виде СО2. Следовательно, подкласс фермента - углерод-углерод-лиазы (см. раздел 2.3). |
|
ОБНОВЛЕНИЯ
ПОДПИСАТЬСЯ НА РАССЫЛКУ
ПРЕДМЕТЫ
- Анатомия
- Акушерство и гинекология
- БЖД, медицина катастроф
- Биохимия
- Биология
- Гистология
- Гигиена
- Генетика
- Диетология
- Дерматовенерология
- Инфекционные болезни
- Культурология
- Лабораторная диагностика
- Летняя практика
- Лучевая диагностика
- Медицинская информатика
- Микробиология
- Неврология
- Общественное здоровье
- Общий уход
О НАС
«Dendrit» - информационный портал для медицинских работников, студентов медицинских ВУЗов, исследователей и пациентов.
Ваш источник новостей и знаний о здоровье.
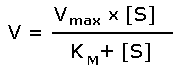 ,
,