ПОДПИСАТЬСЯ НА РАССЫЛКУ
Ответы 1 - 20
1. Первичная структура белка. Зависимость свойств и конформации белков от первичной структуры. Примеры полиморфизма белков, гемоглобин А и F, структурные и функциональные отличия. Роль фетального гемоглобина в период внутриутробного развития плода. Наследственные изменения первичной структуры — молекулярные болезни (серповидно-клеточная анемия).
Первичной структурой белка называют последовательность чередования аминокислот в полипептидной цепи. Эту структуру формируют пептидные связи между α-амино- и α-карбоксильными группами аминокислот (см. 1.4.2). Имейте в виду, что даже небольшие изменения первичной структуры белка могут значительно изменять его свойства. Примером заболеваний, развивающихся в результате изменения первичной структуры белка, являются гемоглобинопатии (гемоглобинозы) .
В эритроцитах здоровых взрослых людей присутствует гемоглобин А (Hb А) . В крови некоторых людей содержится аномальный (изменённый) гемоглобин - гемоглобин (Hb S). Единственное отличие первичной структуры Hb S от Hb A - замена гидрофильного остатка глутаминовой кислоты на гидрофобный остаток валина в концевом участке их β-цепей.
Как известно, основная функция гемоглобина -транспорт кислорода к тканям. В условиях пониженного парциального давления О2 снижается растворимость гемоглобина S в воде и его способность связывать и переносить кислород. Эритроциты принимают при этом серповидную форму, быстро разрушаются, вследствие чего развивается малокровие (серповидно-клеточная анемия] .
Установлено, что последовательность аминокислотных остатков полипептидной цепи белка несёт в себе информацию, необходимую для формирования пространственной структуры белка. Установлено, что каждой полипептидной последовательности соответствует только один стабильный вариант пространственной структуры. Процесс сворачивания полипептидной цепи в правильную трёхмерную структуру получил название фолдинг.
До последнего времени считалось, что формирование пространственной структуры белка происходит самопроизвольно, без участия каких-либо компонентов. Однако сравнительно недавно обнаружилось, что это справедливо только для сравнительно небольших белков (порядка 100 аминокислотных остатков). В процессе фолдинга более крупных белков принимают участие специальные протеины - шапероны, которые создают возможность быстрого формирования правильной пространственной структуры белка.
Примером полиморфизма белков является гемоглобин, имеющий множество форм. Гемоглоби́н A— нормальный гемоглобин взрослого человека. Этот белок представляет собой тетрамер, состоящий из двух пар полипептидных цепей — мономеров: двух мономеров α-цепей и двух мономеров β-цепей, или двух мономеров α и двух мономеров δ. Гемоглоби́н F— фетальный, плодный тип гемоглобина человека. Гемоглобин F — это белок-гетеротетрамер из двух α-цепей и двух γ-цепей глобина. Гемоглобин F обладает повышенным сродством к кислороду(в нём серин вместо лизина) и позволяет сравнительно малому объёму крови плода выполнять кислородоснабжающие функции более эффективно. Однако гемоглобин F обладает меньшей стойкостью к разрушению и меньшей стабильностью. В течение последнего триместра беременности и после рождения гемоглобин F постепенно — замещается «взрослым» гемоглобином А (HbA), менее активным транспортёром кислорода, но более стойким к разрушению и более стабильным. Молекулярные болезни – наследственные нарушения в первичной структуре булка. Например, замена в β-субъединице гемоглобина шестой глутаминовой аминокислоты на валин приводит к образованию гемоглобина S и тому, что молекула гемоглобина в целом не может выполнять свою основную функцию — транспорт кислорода; в таких случаях у человека развивается заболевание — серповидноклеточная анемия.
2. Конформация белковой молекулы (вторичная и третичная структуры). Типы внутримолекулярных связей в белках. Фибриллярные и глобулярные белки (примеры). Четвертичная структура белка. Примеры строения и функционирования олигомерных белков.
Вторичная структура белка представляет собой способ свёртывания полипептидной цепи в спиральную или иную конформацию. При этом образуются водородные связи между СО-и NH-группами пептидного остова одной цепи или смежных полипептидных цепей. Известно несколько типов вторичной структуры пептидных цепей, среди которых главными являются α-спираль и β-складчатый слой.
α-Спираль - жёсткая структура, имеет вид стержня. Внутреннюю часть этого стержня создаёт туго закрученный пептидный остов, радикалы аминокислот направлены наружу. При этом СО-группа каждого аминокислотного остатка взаимодействует с NH-группой четвёртого от него остатка. На один виток спирали приходится 3,6 аминокислотных остатка, а шаг спирали составляет 0,54 нм (рисунок 2.1).
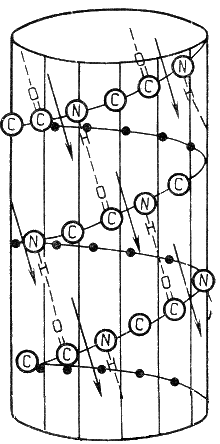
Рисунок 2.1. α-Спираль.
Некоторые аминокислоты препятствуют свёртыванию цепи в α-спираль, и в месте их расположения непрерывность спирали нарушается. К этим аминокислотам относятся пролин (в нём атом азота входит в состав жёсткой кольцевой структуры и вращение вокруг связи N - Сα становится невозможным) , а также аминокислоты с заряженными радикалами, которые электростатически или механически препятствуют формированию α-спирали. Если в пределах одного витка (примерно 4 аминокислотных остатка) находятся два таких радикала (или более), они взаимодействуют и деформируют спираль.
β-Складчатый слой отличается от α-спирали тем, что имеет плоскую, а не стержневидную форму. Образуется при помощи водородных связей в пределах одной или нескольких полипептидных цепей. Пептидные цепи могут быть расположены в одном направлении (параллельно) или в противоположных направлениях (антипараллельно) , напоминая меха аккордеона. Боковые радикалы находятся выше и ниже плоскости слоя.
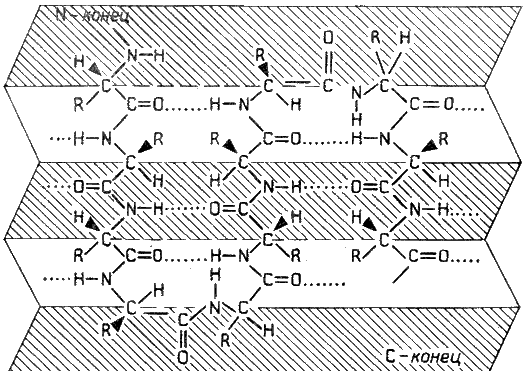
Рисунок 2.2. β-Складчатый слой.
Обратите внимание на то, что тип вторичной структуры белка определяется его первичной структурой. Например, в месте расположения остатка пролина (атомы пирролидинового кольца в пролине лежат в одной плоскости) пептидная цепь делает изгиб, и водородные связи между аминокислотами не образуются. Поэтому белки с высоким содержанием пролина (например, коллаген) не способны образовывать а-спираль. Радикалы аминокислот, несущие электрический заряд, также препятствуют спирализации.
2.1.3. Третичная структура белка - это распределение в пространстве всех атомов белковой молекулы, или иначе говоря, пространственная упаковка спирализованной полипептидной цепи. Основную роль в образовании третичной структуры белка играют водородные, ионные, гидрофобные и дисульфидные связи, которые образуются в результате взаимодействия между радикалами аминокислот.
- Водородные связи образуются между двумя полярными незаряженными радикалами или между незаряженным и заряженным радикалами, например, радикалами серина и глутамина:
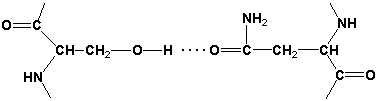
- Ионные связи могут возникать между противоположно заряженными радикаламинапример, радикалами глутамата и аргинина:
- Гидрофобные взаимодействия характерны для неполярных радикалов, например, валина и лейцина:
- Дисульфидные связи образуются между SH-группами двух радикалов цистеина, находящихся в разных участках полипептидной цепи:
.
По форме молекулы и особенностям формирования третичной структуры белки делят на глобулярные и фибриллярные.
Глобулярные белки - имеют сферическую или эллипсовидную форму молекулы (глобула). В процессе образования глобулы гидрофобные радикалы аминокислот погружаются во внутренние области, гидрофильные радикалы располагаются на поверхности молекулы. При взаимодействии с водной фазой полярные радикалы образуют многочисленные водородные связи. Белки удерживаются в растворённом состояния за счёт заряда и гидратной оболочки. В организме глобулярные белки выполняют динамические функции (транспортную, ферментативную, регуляторную, защитную). К глобулярным белкам относятся:
- Альбумин - белок плазмы крови; содержит много остатков глутамата и аспартата; осаждается при 100%-ном насыщении раствора сульфатом аммония.
- Глобулины - белки плазмы крови; по сравнению с альбумином оббладают большей молекулярной массой и содержат меньше остатков глутамата и аспартата, осаждаются при 50%-ном насыщении раствора сульфатом аммония.
- Гистоны - входят в состав ядер клеток, где образуют комплекс с ДНК. Содержат много остатков аргинина и лизина.
Фибриллярные белки - имеют нитевидную форму (фибриллы) , образуют волокна и пучки волокон. Между соседними полипептидными цепями имеется много поперечных ковалентных сшивок. Нерастворимы в воде. Переходу в раствор препятствуют неполярные радикалы аминокислот и сшивки между пептидными цепями. В организме выполняют главным образом структурную функцию, обеспечивают механическую прочность тканей. К фибриллярным белкам относятся:
- Коллаген - белок соединительной ткани. В его составе преобладают аминокислоты глицин, пролин, гидроксипролин.
- Эластин - более эластичен, чем коллаген, входит в состав стенок артерий, лёгочной ткани, в его составе преобладают аминокислоты глицин, аланин, валин.
- Кератин - белок эпидермиса и производных кожи, в его структуре преобладает аминокислота цистеин.
3. Гемоглобин - аллостерический белок. Конформационные изменения молекулы гемоглобина. Кооперативный эффект. Регуляторы сродства гемоглобина к кислороду. Структурные и функциональные различия миоглобина и гемоглобина.
К гемопротеинам относятся: гемоглобин, миоглобин, цитохромы, пероксидаза, каталаза. Эти белки содержат в качестве простетической группой гем.
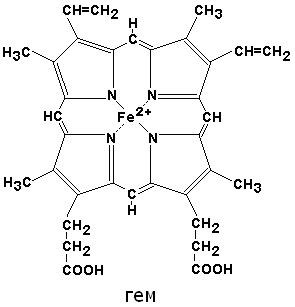
По своему химическому строению гем представляет собой протопорфирин IX, связанный с двухвалентным железом. Протопорфирин IX - органическое соединение, относящееся к классу порфиринов. Протопорфирин IX содержит четыре замещённых пиррольных кольца, соединённых метиновыми мостиками =СН—. Заместителями в пиррольных кольцах являются: четыре метильные группы СН3—, две винильные группы СН2=СН— и два остатка пропионовой кислоты — СН2—СН2—СООН. Гем соединяется с белковой частью следующим образом. Неполярные группы . протопорфирина IX взаимодействуют с гидрофобными участками аминокислот при помощи гидрофобных связей. Кроме того, имеется координационная связь между атомом железа и имидазольным радикалом гистидина в белковой цепи. Ещё одна координационная связь атома железа может использоваться для связывания кислорода и других лигандов.
Присутствие в биологическом материале гемсодержащих белков обнаруживается при помощи бензидиновой пробы (при добавлении бензидина и пероксида водорода исследуемый раствор окрашивается в сине-зелёный цвет).
равните структуру и функцию миоглобина и гемоглобина, запомните характерные особенности каждого из этих белков.
Миоглобин - хромопротеин, присутствующий в мышечной ткани и обладающий большим сродством к кислороду. Молекулярная масса этого белка около 16000 Да, Молекула миоглобина имеет третичную структуру и представляет собой одну полипептидную цепь, соединённую с гемом. Миоглобин не обладает аллостерическими свойствами (см. 2.4.), кривая насыщения его кислородом имеет вид гиперболы (рисунок 4). Функция миоглобина заключается в создании в мышцах кислородного резерва, который расходуется по мере необходимости, восполняя временную нехватку кислорода.
Гемоглобин (Hb) - хромопротеин, присутствующий в эритроцитах и участвующий в транспорте кислорода к тканям. Гемоглобин взрослых людей называется гемоглобином А (Hb A). Молекулярная масса его составляет около 65000 Да. Молекула Hb А имеет четвертичную структуру и включает четыре субъединицы - полипептидные цепи (обозначаемые α1, α2, β1 и β2, каждая из которых связана с гемом.
Запомните, что гемоглобин относится к аллостерическим белкам, его молекулы могут обратимо переходить из одной конформации в другую. При этом изменяется сродство белка к лигандам. Конформация, обладающая наименьшим сродством к лиганду, называется напряжённой, или Т-конформацией. Конформация, обладающая наибольшим сродством к лиганду, называется релаксированной, или R-конформацией.
Различные факторы среды могут сдвигать это равновесие в ту или иную сторону. Аллостерическими регуляторами, влияющими на сродство Hb к O2, являются: 1) кислород; 2) концентрация Н+ (рН среды); 3) углекислота (СO2) ; 4) 2,3-дифосфоглицерат (ДФГ) . Присоединение молекулы кислорода к одной из субъединиц гемоглобина способствует переходу напряжённой конформации в релаксированную и повышает сродство к кислороду других субъединиц той же молекулы гемоглобина. Это явление получило название кооперативного эффекта. Сложный характер связывания гемоглобина с кислородом отражает кривая насыщения гемоглобина O2, имеющая S-образную форму (рисунок 3.1).
Повышение содержания СO2, Н+, ДФГ на фоне низкого парциального давления O2 в тканях способствует взаимодействию этих факторов с гемоглобином и переходу R-конформации в Т-конформацию. Это приводит к смещению равновесия в уравнении (1) вправо. Выделившийся O2 поступает в ткани.
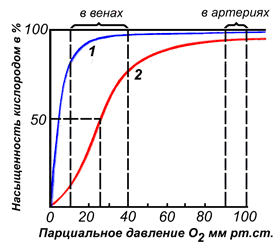
Рисунок 3.1. Кривые насыщения миоглобина (1) и гемоглобина (2) кислородом.
4. Биологические функции белков. Роль пространственной организации полипептидной цепи в образовании активных центров. Взаимодействие белков с лигандами. Денатурация белков.
Белки играют важнейшую роль в организме, выполняя многообразные биологические функции.Запомните наиболее важные из них и примеры соответствующих белков, изучив таблицу 2.2.
|
Таблица 2.2 |
||||||||||||||||||||||||
2.2.2. Обратите внимание на то, что в основе функционирования любого белка лежит его способность к избирательному взаимодействию со строго определёнными молекулами или ионами (лигандами) . Например, для ферментов, катализирующих химические реакции, лигандами будут вещества, участвующие в этих реакциях (субстраты), для транспортных белков - транспортируемые вещества и т.д. 2.2.3. Лиганд способен взаимодействовать не со всей поверхностью белковой молекулы, а только с определённым её участком, который представляет собой центр связывания или активный центр. Этот центр формируется пространственно сближенными радикалами аминокислот на уровне вторичной или третичной структуры белка. Способность лиганда взаимодействовать с центром связывания обусловлена их комплементарностью, то есть взаимным соответствием их пространственной структуры (подобно взаимодействию «ключ - замок»). Между функциональными группами лиганда и центра связывания образуются нековалентные (водородные, ионные, гидрофобные), а также ковалентные связи. Комплементарностью лиганда и центра связывания можно объяснить высокую специфичность (избирательность) взаимодействия белок - лиганд. Важно отметить, что изменение пространственной структуры белка в процессе денатурации (см. 2.4) приводит к разрушению центров связывания и утрате биологической функции белка. |
Денатурацией белков называется это изменение нативных (природных) физико-химических и, главное, биологических свойств белка вследствие нарушения его четвертичной, третичной и даже вторичной структуры. Денатурацию белка могут вызвать:
- температура выше 60° С;
- ионизирующая радиация;
- концентрированные кислоты и щёлочи;
- соли тяжёлых металлов (ртути, свинца, кадмия);
- органические соединения (спирты, фенолы, кетоны) .
Для денатурированных белков характерно:
- изменение конформации молекулы;
- уменьшение растворимости в воде;
- изменение заряда молекулы;
- меньшая устойчивость к действию протеолитических ферментов;
- потеря биологической активности.
Обратите внимание, что при определённых условиях возможно восстановление исходной (нативной) конформации белка после удаления фактора, вызвавшего денатурацию. Этот процесс получил название ренаживации.
Запомните некоторые примеры использования процесса денатурации белков в медицине:
- для осаждения белков плазмы крови при определении содержания небелковых веществ в крови;
- при проведении дезинфекции и санитарной обработки;
- при лечении и профилактике отравлений солями тяжёлых металлов (в качестве противоядия применяют молоко или яичный белок);
- для получения лекарственных веществ белковой природы (используется денатурация в мягких условиях с последующей ренативацией).
5. Строение и биологическая роль нуклеотидов.
|
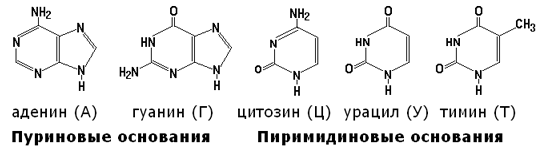
Нуклеиновыми кислотами или полинуклеотидами называются высокомолекулярные вещества, состоящие из нуклеотидов, соединённых в цепь 3', 5'-фосфодиэфирными связями. Каждый нуклеотид состоит из азотистого основания, углевода (пентозы) и остатка фосфорной кислоты. Азотистые основания, входящие в состав нуклеотидов, имеют следующее строение:
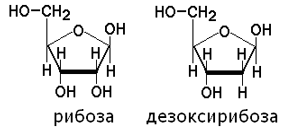
Углеводы представлены рибозой и дезоксирибозой:
4.1.2. Азотистое основание и пентоза, соединённые N-гликозидной связью, образуют нуклеозид. Если в качестве пентозы в нуклеозиде присутствует рибоза, то это рибонуклеозид, а если дезоксирибоза - то это дезоксирибонуклеозид. |
4.1.3. Нуклеотиды представляют собой фосфорилированные нуклеозиды. Остаток фосфорной кислоты, как правило, присоединяется к гидроксильной группе пентозы в 5'-положении при помощи сложноэфирной связи. Примеры:
В клетках встречаются также нуклеозиддифосфаты и нуклеозидтрифосфаты, содержащие соответственно два и три остатка фосфорной кислоты. Биологическая роль этих соединений будет рассматриваться в дальнейшем.
6. Первичная и вторичная структуры ДНК. Правила Чаргаффа. Принцип комплементарности. Типы связей в молекуле ДНК. Биологическая роль ДНК. Молекулярные болезни - следствие генных мутаций.
Первичной структурой нуклеиновых кислот называется последовательность расположения мононуклеотидов в цепи ДНК или РНК. Первичная структура нуклеиновых кислот стабилизируется 3',5'-фосфодиэфирными связями. Эти связи образуются при взаимодействии гидроксильной группы в 3'-положении пентозного остатка каждого нуклеотида с фосфатной группой соседнего нуклеотида (рисунок 3.2),
Таким образом, на одном конце полинуклеотидной цепи имеется свободная 5'-фосфатная группа (5'-конец), а на другом - свободная гидроксильная группа в 3'-положении (3'-конец). Нуклеотидные последовательности принято записывать в направлении от 5'-конца к 3'-концу.
ДНК (дезоксирибонуклеиновая кислота) содержится в клеточном ядре и имеет молекулярную массу порядка 1011 Да. В состав её нуклеотидов входят азотистые основания аденин, гуанин, цитозин, тимин, углевод дезоксирибоза и остатки фосфорной кислоты. Содержание азотистых оснований в молекуле ДНК определяют правила Чаргаффа:
1) количество пуриновых оснований равно количеству пиримидиновых (А + Г = Ц + Т) ;
2) количество аденина и цитозина равно количеству тимина и гуанина соответственно (А = Т; Ц = Г) ;
3) ДНК, выделенные из клеток различных биологических видов, отличаются друг от друга величиной коэффициента специфичности:
(Г + Ц) /(А + Т)
Эти закономерности в строении ДНК объясняются следующими особенностями её вторичной структуры:
1) молекула ДНК построена из двух полинуклеотидных цепей, связанных между собой водородными связями и ориентированных антипараллельно (то есть 3'-конец одной цепи расположен напротив 5'-конца другой цепи и наоборот);
2) водородные связи образуются между комплементарными парами азотистых оснований. Аденину комплементарен тимин; эта пара стабилизируется двумя водородными связями. Гуанину комплементарен цитозин; эта пара стабилизируется тремя водородными связями (см. рисунок б) . Чем больше в молекуле ДНК пар Г-Ц, тем больше её устойчивость к действию высоких температур и ионизирующего излучения;
3) обе цепи ДНК закручены в спираль, имеющую общую ось. Азотистые основания обращены внутрь спирали; кроме водородных, между ними возникают также гидрофобные взаимодействия. Рибозофосфатные части расположены по периферии, образуя остов спирали (см. рисунок 3.4).
Рисунок 3.4. Схема строения ДНК. 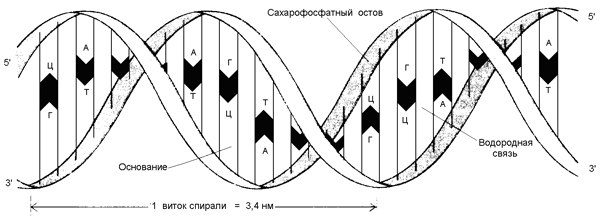
7. Первичная и вторичная структуры РНК. Типы РНК: особенности строения. Основные компоненты белоксинтезирующей системы. Функция рибосом. Адапторная функция тРНК и роль мРНК в синтезе белка.
РНК (рибонуклеиновая кислота) содержится преимущественно в цитоплазме клетки и имеет молекулярную массу в пределах 104 - 106 Да. В состав её нуклеотидов входят азотистые основания аденин, гуанин, цитозин, урацил, углевод рибоза и остатки фосфорной кислоты. В отличие от ДНК, молекулы РНК построены из одной полинуклеотидной цепи, в которой могут находиться комплементарные друг другу участки (рисунок 3.5). Эти участки могут взаимодействовать между собой, образуя двойные спирали, чередующиеся с неспирализованными участками.
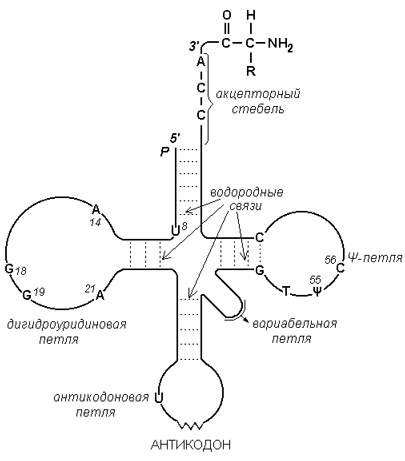
Рисунок 3.5. Схема строения транспортной РНК.
По особенностям структуры и функции различают три основных типа РНК:
1) матричные (информационные) РНК (мРНК) передают информацию о структуре белка из клеточного ядра на рибосомы;
2) транспортные РНК (тРНК) осуществляют транспорт аминокислот к месту синтеза белка;
3) рибосомальные РНК (рРНК) входят в состав рибосом, участвуют в синтезе белка.
8. Биосинтез ДНК (репликация) и мРНК (транскрипция). Процессы "созревания" первичного транскрипта при образовании мРНК.
Матричный биосинтез – процесс сборки новых макромолекул из мономеров, последовательность которых запрограммирована с помощью нуклеиновых кислот. Молекулы, используемые в качестве программы в матричном биосинтезе, называют матрицами.
Тремя главными матричными биосинтезами, присущими всем без исключения живым организмам, являются репликация ДНК, транскрипция и трансляция.
- репликация ДНК происходит в ядре, предшествует делению клеток, в результате чего дочерние клетки получают полный набор генов;
- транскрипция также осуществляется в ядре, в ходе её образуются матричные, транспортные и рибосомальные РНК, участвующие в синтезе белка в клетке;
- трансляция происходит на рибосомах и приводит к образованию специфических клеточных белков.
Связь этих процессов отражена в основном постулате молекулярной биологии: направление потока информации от генотипа к фенотипу: ДНК → РНК → белок (стрелки обозначают направление передачи информации).
4.3.2. Кроме того, для некоторых видов вирусов характерны ещё два вида матричных синтезов:
- репликация РНК – синтез РНК на матрице РНК;
- обратная транскрипция – синтез ДНК с использованием в качестве матрицы молекулы РНК.
4.3.3. Попытаемся сформулировать общие закономерности, характерные для всех матричных биосинтезов.
- Мономеры (нуклеотиды, аминокислоты) непосредственно в синтезе полимеров участвовать не могут; они должны находиться в активной форме – нуклеотиды – в виде нуклеозидтрифосфатов, аминокислоты – в виде соединений с тРНК.
- Синтез всех полинуклеотидных и полипептидных цепей складывается из трёх основных этапов – инициации, элонгации и терминации.
- На матрице имеется специальный сигнал или группа сигналов, позволяющие опознать кодирующий элемент, с которого начинается информация о синтезируемой цепи биополимера. Этот сигнал, как правило, не совпадает с точкой физического начала полимерной цепи матрицы. Инициация – процесс, в котором происходит присоединение первого мономерного звена к молекуле-матрице.
- На каждый акт инициации биосинтеза приходится большое количество актов элонгации, т.е. соединения очередного мономера с растущей цепью. В элонгации участвуют 3 компонента: а) концевая группа синтезируемого полимера, б) кодирующий элемент матрицы, в) очередная молекула активного мономера. Все они должны быть зафиксированы определённым образом в активном центре фермента или рибосомы.
- Каждый акт элонгации начинается с отбора субстратов путём перебора всех присутствующих субстратов в системе. Попадание в активный центр нужного субстрата является сигналом для осуществления ферментативной реакции соединения мономерного фрагмента с концом синтезируемой полимерной цепи. Присоединение мономера к растущей цепи служит сигналом для перемещения активного центра на один кодирующий элемент матрицы.
- Конец продукта чаще всего не соответствует концу матрицы, на ней должен быть специальный сигнал, обеспечивающий прекращение роста цепи, т.е. терминацию.
- Синтез биологически активной молекулы, как правило, не заканчивается терминацией. Образующийся полимер претерпевает ряд превращений, таких как частичный гидролиз и объединение нескольких цепей в одну, модификация мономеров в составе полимера, присоединение простетической части (к полипептиду) или апопротеина (к полинуклеотиду).
Репликация – процесс самоудвоения ДНК, или биосинтез дочерней молекулы ДНК, полностью идентичной исходной молекуле (матрице). Локализация процесса – клеточное ядро. Основные принципы репликации ДНК:
- комплементарность - синтезируемые цепи комплементарны матрице;
- антипараллельность - 5'-конец синтезируемой полинуклеотидной цепи находится напротив 3'-конца матрицы и наоборот;
- униполярность - синтез полинуклеотидных цепей происходит всегда в направлении 5' → 3';
- потребность в затравке - ферменты, синтезирующие ДНК, способны лишь наращивать существующую полинуклеотидную цепь, поэтому вначале синтезируется короткая цепь РНК (затравка или праймер), к которой присоединяются дезоксирибонуклеотиды; выполнившая свою роль РНК-затравка удаляется;
- прерывистость - одна из дочерних цепей (лидирующая) в процессе репликации растёт непрерывно, а другая (отстающая) - в виде фрагментов длиной в несколько сот нуклеотидов (фрагментов Оказаки);
- полуконсервативность - в результате репликации образуются две двойные дочерние ДНК, каждая из которых сохраняет (консервирует) в неизменном виде одну из половин материнской ДНК.
4.4.2. Условия, необходимые для репликации ДНК:
1) Матрица – молекула ДНК (рисунок 26.1, а);
2) Расплетающие белки – разрывают водородные связи между комплементарными основаниями двойной спирали ДНК, в результате чего образуется репликативная вилка (рисунок 26.1, б);
3) ДНК-связываюшие белки - присоединяются к разделившимся цепям ДНК и препятствуют их обратному воссоединению;
4) Праймаза (РНК-полимераза) - фермент, синтезирующий затравочную РНК.
5) Субстраты и источники энергии – дезоксирибонуклеозидтрифосфаты (дАТФ, дГТФ, дТТФ, дЦТФ). Присоединяются к азотистым основаниям полинуклеотидных цепей при помощи водородных связей по принципу комплементарности;
6) ДНК-полимераза – фермент, который формирует из нуклеозидтрифосфатов новые полинуклеотидные цепи за счёт образования 3’,5’-фосфодиэфирных связей. Источником энергии служат макроэргические связи нуклеозидтрифосфатов. На одной ветви репликативной вилки синтезируется непрерывная цепь, на другой – фрагменты Оказаки (рисунок 26.1, в);
7) ДНК-лигаза – фермент, соединяющий фрагменты Оказаки в единую цепь (рисунок 26.1, г).
В результате образуются две идентичные молекулы ДНК (рисунок 26.1, д).
Транскрипция – биосинтез РНК на матрице ДНК. Процесс транскрипции также происходит в клеточном ядре. Основные принципы транскрипции:
- комплементарность - синтезируемые цепи комплементарны матрице;
- антипараллельность - 5'-конец синтезируемой полинуклеотидной цепи находится напротив 3'-конца матрицы и наоборот;
- униполярность - синтез полинуклеотидных цепей происходит всегда в направлении 5' → 3';
- беззатравочность - биосинтез РНК не требует наличия праймера;
- асимметричность - синтез дочерней цепи идёт только на одной цепи ДНК-матрицы, вторая при этом блокирована.
4.5.2. Условия, необходимые для транскрипции:
- Матрица – участок одной из цепей ДНК (рисунок 8.2, а);
- ДНК-зависимая РНК-полимераза – главный фермент, участвующий в транскрипции. Место присоединения фермента к ДНК – промотор;
- Субстраты и источники энергии – рибонуклеозидтрифосфаты (АТФ, ГТФ, УТФ, ЦТФ). Связываются с азотистыми основаниями транскрибируемой цепи ДНК водородными связями по принципу комплементарности.
9. Биосинтез белков. Генетический код. Последовательность реакций при синтезе полипептидной цепи (инициация, элонгация, терминация) в процессе трансляции на рибосомах. Посттрансляционная модификация молекул белков. Нарушения синтеза белка в детском возрасте (квашиоркор).
|
Трансляция (от англ. translation – перевод) – перевод генетической информации, заключённой в мРНК, в линейную последовательность аминокислот в полипептидной цепи. Этот перевод осуществляется посредством генетического (биологического) кода. 5.1.2. Генетический код – последовательность нуклеотидов, соответствующая определённым аминокислотам. Генетический код характеризуется свойствами:
5.1.3. Аминокислоты и триплеты нуклеотидов, кодирующие их, не комплементарны друг другу. Поэтому должны существовать молекулы-адапторы, каждая из которых может взаимодействовать как с определённым кодоном, так и с соответствующей аминокислотой. Такими молекулами являются транспортные РНК (рисунок 8.3). Каждая тРНК содержит триплет нуклеотидов – антикодон, который комплементарен строго определённому кодону мРНК. 3’-конец тРНК (акцепторный участок) является местом присоединения аминокислоты, соответствующей кодону мРНК. |
Активация аминокислот – подготовительный этап биосинтеза белка – включает связывание их со специфическими тРНК при участии фермента аминоацил-тРНК-синтетазы. Реакция происходит в цитоплазме клеток.
Собственно процесс трансляции включает 3 стадии – инициации, элонгации, терминации и происходит на рибосомах.
Каждая рибосома состоит из большой и малой субчастиц (40S и 60S) и содержит аминоацильный (А) и пептидильный (П) участки. Пептидильный участок связывает инициирующую аминоацил-тРНК, все остальные аминоацил-тРНК присоединяются к аминоацильному участку.
1) Стадия инициации – начало трансляции. Условия, необходимые для инициации:
- инициирующий кодон мРНК (АУГ);
- белковые факторы инициации;
- малая и большая субчастицы рибосомы;
- ГТФ (источник энергии для смыкания субчастиц рибосомы);
- ионы магния;
- инициирующая аминоацил-тРНК (метионил-тРНК) – связывается своим антикодоном с инициирующим кодоном мРНК в пептидильном участке рибосомы.
В результате образуется инициирующий комплекс: мРНК – рибосома – метионил-тРНК (рисунок 5.3, а).
2) Стадия элонгации – удлинение полипептидной цепи на 1 аминокислотный остаток – происходит в три шага:
- присоединение к инициирующему комплексу аминоацил-тРНК, соответствующей кодону, находящемуся в аминоацильном участке рибосомы (рисунок 5.3, б);
- транспептидация – образование пептидной связи между остатками аминокислот (рисунок 5.3, в). Источник энергии – ГТФ;
- транслокация – перемещение рибосомы относительно мРНК на 1 триплет (рисунок 5.3, г). Источник энергии – ГТФ. В ходе элонгации принимают участие белковые факторы.
Описанный процесс многократно повторяется (по количеству аминокислот в цепи).
3) Стадия терминации – окончание трансляции. Обеспечивается присутствием в цепи мРНК одного из терминирующих (бессмысленных) кодонов – УАА, УГА или УАГ. В освобождении полипептида участвуют белковые факторы терминации (рисунок 5.3, д). Когда в аминоацильном участке оказывается один из бессмысленных кодонов, факторы терминации стимулируют гидролазную активность пептидилтрансферазы. Благодаря этому гидролизуется связь между тРНК и пептидом. ГТФ для этой реакции не требуется. После этого пептидная цепь, тРНК и мРНК покидают рибосому, а её субчастицы диссоциируют.
Таким образом, трансляция мРНК приводит к формированию пептидной цепи со строго определённой последовательностью аминокислотных остатков. Следующий этап формирования белка –фолдинг, т.е. сворачивание пептидной цепи в правильную трёхмерную структуру. Если белок состоит из нескольких субъединиц, то фолдинг включает и объединение их в единую макромолекулу.
Считается, что небольшие белковые молекулы, содержащие около 100 аминоацильных остатков, могут самостоятельно принимать трёхмерную структуру, фолдинг более крупных полипептидных цепей требует участия специальных белков – шаперонов.
Шапероны называют иначе белками теплового шока, так как они не только обеспечивают правильный фолдинг вновь образованных белков, но и ренатурацию ранее синтезированных белков, подвергшихся в клетке частичной денатурации под действием различных факторов (перегрев, облучение, действие своблодных радикалов и т.д.).
5.2.2. Посттрансляционные модификации белковой молекулы могут включать:
- частичный протеолиз (например, превращение профермента в фермент);
- присоединение простетической группы (остатков фосфорной кислоты, углеводных остатков, гемовых групп и т.д.);
- модификации боковых цепей аминокислотных остатков:
- гидроксилирование пролина в гидроксипролин в коллагене,
- метилирование аргинина в гистоне,
- йодирование тирозина в тироглобулине).
5.2.3. Действие токсических и лекарственных веществ на биосинтез белка. Биосинтез белка является одним из наиболее сложных процессов, протекающих в клетках. Его прерывание или извращение возможно в результате нарушения любого из трёх матричных синтезов.
Так, мутагены (бенз(а)пирен, линдан) нарушают репликацию ДНК и таким образом прерывают белоксинтезирующие процессы.
Некоторые токсические вещества (госсипол) могут изменять скорость транскрипции.
К лекарственным веществам, влияющим на биосинтез белка, относятся антибиотики и интерфероны.
Антибиотики, блокирующие матричные биосинтезы, используются в лечении инфекционных заболеваний и злокачественных опухолей. (см. таблицу 5.1).
Таблица 5.1
Антибиотики, ингибирующие матричные биосинтезы
|
Антибиотики |
Механизм действия |
|
Противоопухолевые препараты: актиномицин Д, рубомицин С, митомицин С |
Подавляют репликацию или транскрипцию, или оба эти процесса |
|
Противобактериальные препараты: тетрациклин, левомицетин, эритромицин, стрептомицин |
Ингибируют трансляцию в бактериальных (но не эукариотических) клетках |
10. Регуляция синтеза белка. Представление об опероне. Индукция и репрессия синтеза в организме человека. Роль гормонов в регуляции действия генов. Ингибиторы матричных синтезов - антибиотики, интерфероны.
|
5.3.1. Оперон (транскриптон) - совокупность генов, способных включаться и выключаться в зависимости от метаболических потребностей клетки. В состав оперона наряду соструктурными генами (СГ), кодирующими структуру определённых белков, входят участки ДНК, выполняющие регуляторные функции (рисунок 5.4). Группа структурных генов, отвечающих за синтез ферментов одного метаболического пути, находится под контролем гена-оператора (ГО), расположенного рядом. Функция гена-оператора контролируется пространственно удалённым от него геном-регулятором (ГР), который продуцирует белок-репрессор, находящийся в активной либо в неактивной форме. Активный белок-репрессор способен связываться с геном-оператором и тормозить транскрипцию структурных генов, следовательно, подавлять синтез белков. Вещества, вызывающие инактивацию белка-репрессора, являются индукторамисинтеза белка, оказывающие противоположный эффект – корепрессорами. В качестве индукторов могут выступать исходные субстраты метаболических путей, в качестве корепрессоров - конечные продукты этих путей. 5.3.2. Существуют два механизма регуляции синтеза белка – индукция и репрессия. Примером оперона, который регулируется по механизму индукции, является лактозный оперон, в состав которого наряду с геном-оператором входят 3 структурных гена, кодирующие ферменты катаболизма лактозы (см. рисунок 5.4). Лактоза является индуктором данного оперона. При высокой концентрации лактозы в среде ферменты синтезируются, при низкой концентрации – нет. |
5.3.3. По механизму репрессии регулируется гистидиновый оперон, содержащий ген-оператор и 10 структурных генов, кодирующих ферменты, необходимые для биосинтеза гистидина (см. рисунок 5.5). Гистидин является корепрессором данного оперона. При высокой концентрации гистидина в среде синтез ферментов прекращается, при отсутствии гистидина они синтезируются.
11. Роль ферментов в метаболизме. Наследственные энзимопатии в раннем детском возрасте. Многообразие ферментов. Специфичность действия ферментов. Классификация ферментов. Изоферменты, мультиферменты.
Протекание процессов обмена веществ в организме определяется действием многочисленных ферментов — биологических катализаторов белковой природы. Они ускоряют химические реакции и сами при этом не расходуются. Термин «фермент» происходит от латинского слова fermentum — закваска. Наряду с этим понятием в литературе используется равноценный термин «энзим» (en zyme - в дрожжах) греческого происхождения. Отсюда раздел биохимии, изучающий ферменты, получил название «энзимология».
Энзимология составляет основу познания на молекулярном уровне важнейших проблем физиологии и патологии человека. Переваривание пищевых веществ и их использование для выработки энергии, образование структурных и функциональных компонентов тканей, сокращение мышц, передача электрических сигналов по нервным волокнам, восприятие света глазом, свертывание крови — каждый из этих физиологических механизмов имеет в основе каталитическое действие определенных ферментов. Было показано, что многочисленные заболевания непосредственно нарушением ферментативного катализа; определение активности ферментов в крови и других тканях даёт ценные сведения для медицинской диагностики; ферменты или их ингибиторы могут применяться как лекарственные вещества. Таким образом, знание важнейших особенностей ферментов и катализируемых ими реакций необходимо при рациональном подходе к изучению заболеваний человека, их диагностике и лечению.
В основу классификации положен важнейший признак, по которому один фермент отличается от другого — это катализируемая им реакция. Число типов химических реакций сравнительно невелико, что позволило разделить все известные в настоящее время ферменты на 6 важнейших классов, в зависимости от типа катализируемой реакции. Такими классами являются:
- оксидоредуктазы (окислительно-восстановительные реакции);
- трансферазы (перенос функциональных групп);
- гидролазы (реакции расщепления с участием воды);
- лиазы (разрыв связей без участия воды);
- изомеразы (изомерные превращения);
- лигазы (синтез с затратой молекул АТФ).
7.4.3. Ферменты каждого класса делят на подклассы, руководствуясь строением субстратов. В подклассы объединяют ферменты, действующие на сходно построенные субстраты. Подклассы разбивают на подподклассы, в которых ещё строже уточняют структуру химических групп, отличающих субстраты друг от друга. Внутри подподклассов перечисляют индивидуальные ферменты. Все подразделения классификации имеют свои номера. Таким образом, любой фермент получает свой уникальный кодовый номер, состоящий из четырёх чисел, разделённых точками. Первое число обозначает класс, второе - подкласс, третье - подподкласс, четвёртое - номер фермента в пределах подподкласса. Например, фермент α-амилаза, расщепляющая крахмал, обозначается как 3.2.1.1, где:
3 — тип реакции (гидролиз);
2 — тип связи в субстрате (гликозидная);
1 — разновидность связи (О-гликозидная);
1 — номер фермента в подподклассе
Вышеописанный десятичный способ нумерации имеет одно важное преимущество: он позволяет обойти главное неудобство сквозной нумерации ферментов, а именно: необходимость при включении в список вновь открытого фермента изменять номера всех последующих. Новый фермент может быть помещён в конце соответствующего подподкласса без нарушения всей остальной нумерации. Точно так же при выделении новых классов, подклассов и подподклассов их можно добавлять без нарушения порядка нумерации ранее установленных подразделений. Если после получения новой информации возникает необходимость изменить номера некоторым ферментам, прежние номера не присваивают новым ферментам, чтобы избежать недоразумений.
Говоря о классификации ферментов, следует также отметить, что ферменты классифицируются не как индивидуальные вещества, а как катализаторы определённых химических превращений. Ферменты, выделенные из разных биологических источников и катализирующие идентичные реакции, могут существенно отличаться по своей первичной структуре. Тем не менее в классификационном списке все они фигурируют под одним и тем же кодовым номером.
Итак, знание кодового номера фермента позволяет:
- устранить неоднозначности, если разные исследователи используют одно и то же название для различных ферментов;
- сделать поиск информации в литературных базах данных более эффективным;
- получить в других базах данных дополнительную информацию о последовательности аминокислот, пространственной структуре фермента, генах, кодирующих ферментные белки.
Изоферменты – это множественные формы одного фермента, катализирующие одну и ту же реакцию, но отличающие по физическим и химическим свойствам (сродству к субстрату, максимальной скорости катализируемой реакции, электрофоретической подвижности, разной чувствительности к ингибиторам и активаторам, оптимуму рН и термостабильности). Изоферменты имеют четвертичную структуру, которая образована четным количеством субъединиц (2, 4, 6 и т.д.). Изоформы фермента образуются в результате различных комбинаций субъединиц.
В качестве примера можно рассмотреть лактатдегидрогеназу (ЛДГ), фермент, который катализирует обратимую реакцию:
НАДН2 НАД+
пируват ←ЛДГ→ лактат
ЛДГ существует в виде 5 изоформ, каждая из которых состоит из 4-х протомеров (субъединиц) 2 типов М (muscle) и Н (heart). Синтез протомеров М и Н типа кодируется двумя разными генетическими локусами. Изоферменты ЛДГ различаются на уровне четвертичной структуры: ЛДГ1 (НННН), ЛДГ2 (НННМ), ЛДГ3 (ННММ), ЛДГ4 (НМММ), ЛДГ5 (ММММ).
Полипептидные цепи Н и М типа имеют одинаковую молекулярную массу, но в составе первых преобладают карбоновые аминокислоты, последних – диаминокислоты, поэтому они несут разный заряд и могут быть разделены методом электрофореза.
Кислородный обмен в тканях влияет на изоферментный состав ЛДГ. Где доминирует аэробный обмен, там преобладают ЛДГ1, ЛДГ2 (миокард, надпочечники), где анаэробный обмен - ЛДГ4, ЛДГ5 (скелетная мускулатура, печень). В процессе индивидуального развития организма в тканях происходит изменение содержания кислорода и изоформ ЛДГ. У зародыша преобладают ЛДГ4, ЛДГ5. После рождения в некоторых тканях происходит увеличение содержания ЛДГ1, ЛДГ2.
Существование изоформ повышает адаптационную возможность тканей, органов, организма в целом к меняющимся условиям. По изменению изоферментного состава оценивают метаболическое состояние органов и тканей.
12. Свойства ферментов. Зависимость скорости ферментативной реакции от концентрации фермента и субстрата, температуры и рН среды.
Белковая природа ферментов обусловливает появление у них ряда свойств, в целом нехарактерных для неорганических катализаторов: олигодинамичность, специфичность, зависимость скорости реакции от температуры, рН среды, концентрации фермента и субстрата, присутствия активаторов и ингибиторов.
Под олигодинамичностью ферментов понимают высокую эффективность действия в очень малых количествах. Такая высокая эффективность объясняется тем, что молекулы ферментов в процессе своей каталитической деятельности непрерывно регенерируют. Типичная молекула фермента может регенерировать миллионы раз в минуту. Надо сказать, что и неорганические катализаторы также способны ускорять превращение такого количества веществ, которое во много раз превышает их собственную массу. Но ни один неорганический катализатор не может сравниться с ферментами по эффективности действия.
Примером может служить фермент реннин, вырабатываемый слизистой оболочкой желудка жвачных животных. Одна молекула его за 10 минут при 37°С способна вызывать коагуляцию (створаживание) порядка миллиона молекул казеиногена молока.
Другой пример высокой эффективности ферментов даёт каталаза. Одна молекула этого фермента при 0°С расщепляет за секунду около 50 000 молекул пероксида водорода:
2 Н2О2 2 Н2О + О2
Действие каталазы на пероксид водорода заключается в изменении величины энергии активации этой реакции приблизительно от 75 кДж/моль без катализатора до 21 кДж/моль в присутствии фермента. Если же в качестве катализатора этой реакции используется коллоидная платина, то энергия активации составляет всего 50 кДж/моль.
7.2.2. При изучении влияния какого-либо фактора на скорость ферментативной реакции все прочие факторы должны оставаться неизменными и по возможности иметь оптимальное значение.
Мерой скорости ферментативных реакций служит количество субстрата, подвергшегося превращению в единицу времени, или количество образовавшегося продукта. Изменение скорости проводят на начальной стадии реакции, когда продукт ещё практически отсутствует, и обратная реакция не идёт. Кроме того, на начальной стадии реакции концентрация субстрата соответствует его исходному количеству.
7.2.3. Зависимость скорости ферментативной реакции (V) от концентрации фермента [Е] (рисунок 7.3). При высокой концентрации субстрата (многократно превышающей концентрацию фермента) и при постоянстве других факторовскорость ферментативной реакции пропорциональна концентрации фермента. Поэтому зная скорость реакции, катализируемой ферментом, можно сделать вывод о его количестве в исследуемом материале.
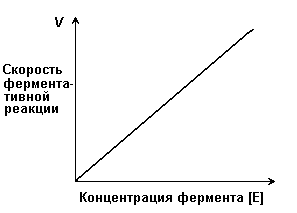
Рисунок 7.3. Зависимость скорости ферментативной реакции от концентрации фермента
7.2.4. Зависимость скорости реакции от концентрации субстрата [S]. График зависимости имеет вид гиперболы (рисунок 7.4). При постоянной концентрации фермента скорость катализируемой реакции возрастает с увеличением концентрации субстрата до максимальной величины Vmax, после чего остаётся постоянной. Это следует объяснить тем, что при высоких концентрациях субстрата все активные центры молекул фермента оказываются связанными с молекулами субстрата. Любое избыточное количество субстрата может соединиться с ферментом лишь после того, как образуется продукт реакции и освободится активный центр.
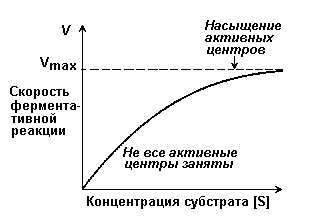
Рисунок 7.4. Зависимость скорости ферментативной реакции от концентрации субстрата.
Зависимость скорости реакции от концентрации субстрата может быть выражена уравнением Михаэлиса — Ментен:
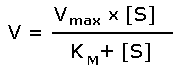 ,
,
где V — скорость реакции при концентрации субстрата [S] , Vmax —максимальная скорость и KM —константа Михаэлиса.
Константа Михаэлиса равна концентрации субстрата, при которой скорость реакции составляет половину максимальной. Определение KM и Vmax имеет важное практическое значение, так как позволяет количественно описать большинство ферментативных реакций, включая реакции с участием двух и более субстратов. Различные химические вещества, изменяющие активность ферментов, по-разному воздействуют на величины Vmax и KM.
7.2.5. Зависимость скорости реакции от t – температуры, при которой протекает реакция (рисунок 7.5), имеет сложный характер. Значение температуры, при котором скорость реакции максимальна, представляет собой температурный оптимум фермента. Температурный оптимум большинства ферментов организма человека приблизительно равен 40°С. Для большинства ферментов оптимальная температура равна или выше тойц температуры, при которой находятся клетки.
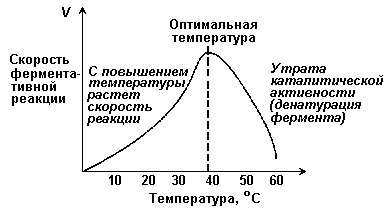
Рисунок 7.5. Зависимость скорости ферментативной реакции от температуры.
При более низких температурах (0° — 40°С) скорость реакции увеличивается с ростом температуры. При повышении температуры на 10°С скорость ферментативной реакции удваивается (температурный коэффициент Q10 равен 2). Повышение скорости реакции объясняется увеличением кинетической энергии молекул. При дальнейшем повышении температуры происходит разрыв связей, поддерживающих вторичную и третичную структуру фермента, то есть тепловая денатурация. Это сопровождается постепенной потерей каталитической активности.
7.2.6. Зависимость скорости реакции от рН среды (рисунок 7.6). При постоянной температуре фермент работает наиболее эффективно в узком интервале рН. Значение рН, при котором скорость реакции максимальна, представляет собой оптимум рН фермента. У большинства ферментов организма человека оптимум рН находится в пределах рН 6 – 8, но есть ферменты, которые активны при значениях рН, лежащих за пределами этого интервала (например, пепсин, наиболее активный при рН 1,5 - 2,5).
Изменение рН как в кислую, так и в щелочную сторону от оптимума приводит к изменению степени ионизации кислых и основных групп аминокислот, входящих в состав фермента (например, СООН-группы аспартата и глутамата, NН2-группы лизина и т.д.). Это вызывает изменение конформации фермента, в результате чего изменяется пространственная структура активного центра и снижение его сродства к субстрату. Кроме того, при экстремальных значениях рН происходит денатурация фермента и его инактивация.
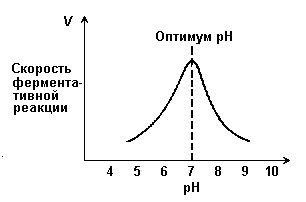
Рисунок 7.6. Зависимость скорости ферментативной реакции от рН среды.
Следует отметить, что свойственный ферменту оптимум рН не всегда совпадает с рН его непосредственного внутриклеточного окружения. Это позволяет предположить, что среда, в которой находится фермент, в какой-то мере регулирует его активность.
7.2.7. Зависимость скорости реакции от присутствия активаторов и ингибиторов. Активаторы повышают скорость ферментативной реакции. Ингибиторы понижают скорость ферментативной реакции.
В качестве активаторов ферментов могут выступать неорганические ионы. Предполагают, что эти ионы заставляют молекулы фермента или субстрата принять конформацию, способствующую образованию фермент-субстратного комплекса. Тем самым увеличивается вероятность взаимодействия фермента и субстрата, а следовательно и скорость реакции, катализируемой ферментом. Так, например, активность амилазы слюны повышается в присутствии хлорид-ионов.
13. Механизм действия ферментов. Каталитический (активный) центр. Коферменты и кофакторы. Конкурентное и неконкурентное ингибирование. Использование конкурентных ингибиторов как лекарственных препаратов.
Активный центр (Ац) – это часть молекулы фермента, которая специфически взаимодействует с субстратом и принимает непосредственное участие в катализе. Ац, как правило, находиться в нише (кармане). В Ац можно выделить два участка: участок связывания субстрата – субстратный участок (контактная площадка) и собственно каталитический центр.
Большинство субстратов образует, по меньшей мере, три связи с ферментом, благодаря чему молекула субстрата присоединяется к активному центру единственно возможным способом, что обеспечивает субстратную специфичность фермента. Каталитический центр обеспечивает выбор пути химического превращения и каталитическую специфичность фермента.
У группы регуляторных ферментов есть аллостерические центры, которые находятся за пределами активного центра. К аллостерическому центру могут присоединяться “+” или “–“ модуляторы, регулирующие активность ферментов.
Различают ферменты простые, состоят только из аминокислот, и сложные, включают также низкомолекулярные органические соединения небелковой природы (коферменты) и (или) ионы металлов (кофакторы).
Коферменты – это органические вещества небелковой природы, принимающие участие в катализе в составе каталитического участка активного центра. В этом случае белковую составляющую называют апоферментом, а каталитически активную форму сложного белка – холоферментом. Таким образом: холофермент = апофермент + кофермент.
В качестве коферментов функционируют:
- гемы,
- нуклеотиды,
- коэнзим Q,
- ФАФС,
- SAM,
- Глутатион
- производные водорастворимых витаминов:
|
Витамины |
Коферменты |
|
РР (никотиновая кислота) |
НАД+, НАДФ+ |
|
В2 (рибофлавин) |
ФАД, ФМН |
|
В6 (пиридоксаль) |
Пиридоксальфосфат |
|
В1 (тиамин) |
Тиаминпирофосфат |
|
В12 |
Кобаламины |
Кофермент, который присоединен к белковой части ковалентными связями называется простетической группой. Это, например, FAD, FMN, биотин, липоевая кислота. Простетическая группа не отделяется от белковой части. Кофермент, который присоединен к белковой части нековалентными связями называется косубстрат. Это, например, НАД+, НАДФ+. Косубстрат присоединяется к ферменту в момент реакции.
Кофакторы ферментов – это ионы металлов, необходимые для проявления каталитической активности многих ферментов. В качестве кофакторов выступают ионы калия, магния, кальция, цинка, меди, железа и т.д. Их роль разнообразна, они стабилизируют молекулы субстрата, активный центр фермента, его третичную и четвертичную структуру, обеспечивают связывание субстрата и катализ. Например, АТФ присоединяется к киназам только вместе с Mg2+.
14. Основные механизмы регуляции действия ферментов и их роль в регуляции метаболизма. Проферменты.
8.4.1. Как уже отмечалось, ферменты, относятся к катализаторам, активность которых может регулироваться. Поэтому через ферменты можно контролировать скорость протекающих химических реакций в организме. Регуляция активности ферментов может осуществляться путем взаимодействия с ними различных биологических компонентов или чужеродных соединений (например, лекарств и ядов), которые принято называть модификаторами или регуляторами ферментов. Под действием модификаторов на фермент реакция может ускоряться (в этом случае их называют активаторами) или замедляться (в этом случае их называют ингибиторами).
8.4.2. Активация ферментов определяется по ускорению биохимических реакций, наступающему после действия модификатора. Одну группу активаторов составляют вещества, влияющие на область активного центра фермента. К ним относятся кофакторы ферментов и субстраты. Кофакторы (ионы металлов и коферменты) являются не только обязательными структурными элементами сложных ферментов, но и по существу их активаторами.
Из ионов металлов на активность многих ферментов влияют: NH4+, Na+, Mg2+, K+, Ca2+, Mn2+, Zn2+, Fe2+, Fe3+, Co2+. Ионы тяжелых металлов, как правило, оказывают ингибирующее влияние. Действие катионов в основном довольно специфично, но в большинстве случаев фермент активируется более, чем одним катионом. Наблюдается также явление антагонизма между ионами. Наиболее известен антагонизм между Na+ и К+ и между Mg2+ и Са2+.
Магний является природным активатором ферментов, действующих на фосфорилированные субстраты (фосфатазы, киназы, синтетазы), но в условиях in vitro может быть заменён марганцем.
Анионы в общем мало влияют на активность ферментов, и их воздействие лишено специфичности. Исключением является амилаза, активируемая хлоридами, а также, в меньшей степени, другими галогенами. Влияние активирующего иона изменяется также в зависимости от рН. Степень очистки фермента также влияет на активирующую концентрацию иона и на специфичность активации. Высокоочищенные ферменты характеризуются большей избирательностью по отношению к активирующим ионам.
8.4.3. Активирующее действие ионов металлов реализуется различными путями. Наиболее типичным механизмом является включение иона в структуру каталитического центра фермента, который без него не проявляет активности. Это типичная функция металла в роли кофермента. Другой, довольно частой функцией активирующего металла является образование связи между ферментом и субстратом, или между ферментом, коферментом и субстратом. Например, ионы Zn2+ в составе фермента алкогольдегидрогеназы образуют 2 координационные связи с молекулой кофермента НАД+, 3 координационные связи с молекулой апофермента, а шестая координационная связь присоединяет субстрат.
Ионы металлов, так же как и субстраты, коферменты, их предшественники и структурные аналоги, можно использовать на практике в качестве препаратов, регулирующих активность ферментов.
Если каталитически активный белок называется ферментом (или энзимом), то неактивный предшественник фермента называется проферментом (или зимогеном).
Активация белков путем частичного протеолиза - процесс, широко распространенный в биологических системах. Вот несколько примеров.
- пищеварительные ферменты, гидролизующие белки, синтезируются в желудке и поджелудочной железе в виде проферментов: пепсин – в виде пепсиногена, трипсин – в виде трипсиногена и т.д.
- свертывание крови представляет собой каскад реакций протеолитической активации проферментов. Это обеспечивает быструю ответную реакцию на повреждение кровеносного сосуда.
- некоторые белковые гормоны синтезируются в виде неактивных предшественников. Например, инсулин образуется из проинсулина.
- фибриллярный белок соединительной ткани коллаген также образуется из предшественника — проколлагена.
15. Принципы количественного определения ферментов. Единицы активности ферментов. Основные направления использования ферментов в медицине. Энзимодиагностика, энзимотерапия, использование ферментов как реагентов.
Уникальное свойство ферментов ускорять химические реакции может быть использовано для количественного определения содержания этих биокатализаторов в биологическом материале (тканевом экстракте, сыворотке крови и т.д.). При правильно подобранных экспериментальных условиях почти всегда существует пропорциональность между количеством фермента и скоростью катализируемой реакции, поэтому по активности фермента можно судить о количественном содержании его в исследуемой пробе.
Измерение ферментативной активности основывается на сравнении скорости химической реакции в присутствии активного биокатализатора со скоростью реакции в контрольном растворе, в котором фермент отсутствует или инактивирован.
Исследуемый материал помещают в инкубационную среду, где созданы оптимальные температура, рН среды, концентрации активаторов и субстратов. Одновременно осуществляют постановку контрольной пробы, в которую фермент не добавляют. Спустя некоторое время реакцию останавливают путём добавления различных реагентов (изменяющих рН среды, вызывающих денатурацию белков и т.д.) и проводят анализ проб.
Для того чтобы определить скорость ферментативной реакции, необходимо знать:
- разность концентраций субстрата или продукта реакции до и после инкубации;
- время инкубации;
- количество материала, взятое для анализа.
Наиболее часто активность фермента оценивают по количеству образовавшегося продукта реакции. Так поступают, например, при определении активности аланинаминотрансферазы, катализирующей следующую реакцию:
Определяя содержание одного из продуктов реакции – пировиноградной кислоты – в пробе после инкубации и вычитая из этого значения количество пировиноградной кислоты в контрольной пробе (в неё исследуемый материал добавляется после инкубации), находят количество продукта реакции, образовавшегося за время инкубации.
Активность фермента можно рассчитывать также исходя из количества израсходованного субстрата. В качестве примера можно привести способ определения активности α-амилазы – фермента, расщепляющего крахмал. Измерив содержание крахмала в пробе до и после инкубации и вычислив разность, находят количество субстрата, расщеплённого за время инкубации.
Существует большое количество методов измерения активности ферментов, различающихся по технике исполнения, специфичности, чувствительности.
Чаще всего для определения применяются фотоэлектроколориметрические методы. В основе этих методов лежат цветные реакции с одним из продуктов действия ферментов. При этом интенсивность окраски получаемых растворов (измеренная на фотоэлектроколориметре) пропорциональна количеству образовавшегося продукта. Например, в процессе реакций, катализируемых аминотрансферазами, накапливаются α-кетокислоты, которые дают с 2,4-динитрофенилгидразином соединения красно-бурого цвета:
Если исследуемый биокатализатор обладает низкой специфичностью действия, то можно подобрать такой субстрат, в результате реакции с которым образуется окрашенный продукт. Примером может служить определение щелочной фосфатазы – фермента, широко распространённого в тканях человека, его активность в плазме крови существенно меняется при заболеваниях печени и костной системы. Этот фермент в щелочной среде гидролизует большую группу фосфорнокислых эфиров, как природных, так и синтетических. Одним из синтетических субстратов является паранитрофенилфосфат (бесцветный), который в щелочной среде расщепляется на ортофосфат и паранитрофенол (жёлтого цвета).
За ходом реакции можно наблюдать, измеряя постепенно нарастающую интенсивность окраски раствора:
Для ферментов, обладающих высокой специфичностью действия, такой подбор субстратов, как правило, невозможен.
Спектрофотометрические методы основаны на изменении ультрафиолетового спектра химических веществ, принимающих участие в реакции. Большинство соединений поглощает ультрафиолетовые лучи, причём поглощаемые длины волн характерны для присутствующих в молекулах этих веществ определённых групп атомов. Ферментативные реакции вызывают внутримолекулярные перегруппировки, в результате которых меняется ультрафиолетовый спектр. Эти изменения можно зарегистрировать на спектрофотометре.
Спектрофотометрическими методами, например, определяют активность окислительно-восстановительных ферментов, содержащих в качестве коферментов НАД или НАДФ. Эти коферменты действуют как акцепторы или доноры атомов водорода и, таким образом, либо восстанавливаются, либо окисляются в процессах метаболизма. Восстановленные формы этих коферментов имеют ультрафиолетовый спектр с максимумом поглощения при 340 нм, окисленные формы этого максимума не имеют. Так, при действии лактатдегидрогеназы на молочную кислоту происходит перенос водорода на НАД, что приводит к увеличению поглощения НАДН при 340 нм. Величина этого поглощения в оптических единицах пропорциональна количеству образовавшейся восстановленной формы кофермента.
По изменению содержания восстановленной формы кофермента можно определить активность фермента.
Флюориметрические методы. В основе этих методов лежит явление флюоресценции, которое заключается в том, что исследуемый объект под влиянием облучения излучает свет с более короткой длиной волны. Флюориметрические методы определения активности ферментов более чувствительны, чем спектрофотометрические. Сравнительно новыми и ещё более чувствительными являются хемилюминесцентные методы с применением люциферин-люциферазной системы. Такие методы позволяют определять скорость реакций, протекающих с образованием АТФ. При взаимодействии люциферина (карбоновой кислоты сложного строения) с АТФ образуется люцифериладенилат. Это соединение окисляется при участии фермента люциферазы, что сопровождается световой вспышкой. Измеряя интенсивность световых вспышек, удаётся определять количества АТФ порядка нескольких пикомолей (10–12 моль).
Титрометрические методы. Ряд ферментативных реакций сопровождается изменением рН инкубационной смеси. Примером такого фермента является липаза поджелудочной железы. Липаза катализирует реакцию:
Образующиеся жирные кислоты могут быть оттитрованы, причём количество щёлочи, израсходованное на титрование, будет пропорционально количеству выделившихся жирных кислот и, следовательно, активности липазы. Определение активности этого фермента имеет клиническое значение.
Манометрические методы основаны на измерении в закрытом реакционном сосуде объёма газа, выделившегося (или поглощённого) в ходе энзиматической реакции. С помощью таких методов были открыты и изучены реакции окислительного декарбоксилирования пировиноградной и α-кетоглутаровой кислот, протекающие с выделением СО2. В настоящее время эти методы используются редко.
Международная комиссия по ферментам предложила за единицу активности любого фермента принимать такое количество фермента, которое при заданных условиях катализирует превращение одного микромоля (10–6 моль) субстрата в единицу времени (1 мин, 1 час) или одного микроэквивалента затронутой группы в тех случаях, когда атакуется более одной группы в каждой молекуле субстрата (белки, полисахариды и другие). Должна быть указана температура, при которой проводится реакция. Результаты измерений активности ферментов могут быть выражены в единицах общей, удельной и молекулярной активности.
За единицу общей активности фермента принимают такое количество фермента, которое катализирует превращение 1 мкмоль субстрата в единицу времени в расчёте на количество материала, взятого для исследования. Так, активность аланинаминотрансферазы в печени крыс равна 1670 мкмоль пирувата в час на 1 г ткани; активность холинэстеразы в сыворотке крови человека составляет 250 мкмоль уксусной кислоты в час на 1 мл сыворотки при 37°C.
Особого внимания исследователя требуют высокие значения активности фермента как в норме, так и в патологии. Рекомендуется работать с небольшими показателями активности фермента. Для этого источник фермента берут в меньшем количестве (сыворотку разводят в несколько раз физиологическим раствором, а для ткани готовят меньший процентный гомогенат). По отношению к ферменту в таком случае создаются условия насыщения субстратом, что способствует проявлению его истинной активности.
Общая активность фермента рассчитывается с помощью формулы:
где а – активность фермента (общая), ΔС – разность концентраций субстрата до и после инкубации; В – количество материала, взятого на анализ, t - время инкубации; n - разведение.
Следует иметь в виду, что показатели активности ферментов сыворотки крови и мочи, исследуемых в диагностических целях, выражают в единицах общей активности.
Поскольку ферменты являются белками, важно знать не только общую активность фермента в исследуемом материале, но и ферментативную активность белка, находящегося в данной пробе. За единицу удельной активности принимают такое количество фермента, которое катализирует превращение 1 мкмоль субстрата в единицу времени в расчёте на 1 мг белка пробы. Для вычисления удельной активности фермента необходимо общую активность разделить на содержание белка в пробе:
Например, содержание белка в ткани печени составляет 160 мг/г. Разделив общую активность аланинаминотрансферазы (см. выше) на это значение, получаем 10,4 мкмоль пирувата/мг белка × час.
Чем хуже очищен фермент, тем больше в пробе находится посторонних балластных белков, тем ниже удельная активность. В ходе очистки количество таких белков уменьшается, и соответственно удельная активность фермента повышается. Предположим, в исходном биологическом материале, являющемся источником фермента (измельчённая печень, кашица из растительной ткани), удельная активность была равна 0,5 мкмоль/ (мг белка× мин). После дробного осаждения сульфатом аммония и гель-фильтрации через сефадекс она повысилась до 25 мкмоль/ (мг белка× мин), т.е. увеличилась в 50 раз. К оценке эффективности очистки ферментных препаратов прибегают при производстве лекарственных средств энзиматической природы.
Удельную активность определяют в том случае, когда нужно сопоставить активность разных препаратов одного и того же фермента. Если требуется сравнить активность разных ферментов, рассчитывают молекулярную активность.
Молекулярная активность (или число оборотов фермента) – это количество моль субстрата, подвергающееся превращению под действием 1 моль фермента в единицу времени (обычно в 1 минуту). Разным ферментам присуща неодинаковая молекулярная активность. Уменьшение числа оборотов ферментов происходит под действием неконкурентных ингибиторов. Изменяя конформацию каталитического центра фермента, эти вещества понижают сродство фермента к субстрату, что приводит к уменьшению числа молекул субстрата, реагирующих с одной молекулой фермента в единицу времени.
16. Питание - составная часть обмена веществ. Основные компоненты пищевого рациона и их роль. Заменимые и незаменимые компоненты пищевого рациона. Сбалансированное питание. Последствия несбалансированного питания у детей.
Полноценным называется рацион, соответствующий энергетическим потребностям человека и содержащий необходимое количество незаменимых пищевых веществ, обеспечивающих нормальный рост и развитие организма.
Факторы, влияющие на потребность организма в энергии и питательных веществах: пол, возраст и масса тела человека, его физическая активность, климатические условия, биохимические, иммунологические и морфологические особенности организма.
Все питательные вещества можно разделить на пять классов:
1. белки; 2. жиры; 3. углеводы; 4. витамины; 5. минеральные вещества.
Кроме того, любая диета должна содержать воду, как универсальный растворитель.
Незаменимыми компонентами пищевого рациона являются:
- незаменимые аминокислоты - валин, изолейцин, лейцин, лизин, метионин, фенилаланин, треонин, триптофан;
- незаменимые (эссенциальные) жирные кислоты - линолевая, линоленовая, арахидоновая;
- водо- и жирорастворимые витамины;
- неорганические (минеральные) элементы - кальций, калий, натрий, хлор, медь, железо, хром, фтор, йод и другие.
11.1.2. Сбалансированный пищевой рацион. Диета, содержащая питательные вещества в соотношении, оптимальном для максимального удовлетворения пластических и энергетических потребностей организма человека, называется сбалансированным пищевым рационом. Считается, что самым благоприятным является соотношение белков, жиров и углеводов близкое к 1:1:4, при условии что общая калорийность рациона соответствует энергозатратам данного человека. Так, для студента-юноши весом 60 кг, энергозатраты составляют в среднем 2900 ккал в сутки и рацион должен содержать: 80-100 г белков, 90 г жиров, 300 - 400 г углеводов.
17. Биологическая ценность пищевых белков. Количество и качество белков в питании человека. Заменимые и незаменимые аминокислоты. Комбинирование пищевых продуктов, взаимодополняющих по аминокислотному составу. Характеристика белковой диеты детей. Последствия недостаточного белкового питания у детей.
Биологическая роль пищевых белков заключается в том, что они служат источником незаменимых и заменимых аминокислот. Аминокислоты используются организмом для синтеза собственных белков; в качестве предшественников небелковых азотистых веществ (гормонов, пуринов, порфиринов и др.); как источник энергии (окисление 1 г белков даёт примерно 4 ккал энергии).
Пищевые белки делятся на полноценные и неполноценные.
Полноценные пищевые белки - животного происхождения, содержат в своём составе все аминокислоты в необходимых пропорциях и хорошо усваиваются организмом.
Неполноценные белки - растительного происхождения, не содержат, или содержат в недостаточном количестве одну или несколько незаменимых аминокислот. Так, зерновые культуры, дефицитны по лизину, метионину, треонину; в белке картофеля мало метионина и цистеина. Для получения полноценных по белку пищевых рационов, следует комбинировать растительные белки, дополняющие друг друга по аминокислотному составу, например, кукурузу и бобы.
Суточная потребность: не менее 50 г в сутки, в среднем 80-100 г.
11.2.2. Белковая недостаточность в детском возрасте вызывает: 1. снижение сопротивляемости организма инфекциям; 2. остановку роста вследствие нарушения синтеза факторов роста; 3. энергетическую недостаточность организма (истощение углеводных и жировых депо, катаболизм тканевых белков); 4. потерю массы тела - гипотрофию. При белковом голодании наблюдаются отеки, которые возникают вследствие снижения содержания белков в крови (гипоальбуминемии) и нарушения распределения воды между кровью и тканями.
18. Переваривание белков. Протеиназы. Механизм активации протеиназ желудочно-кишечного тракта. Специфичность (избирательность) гидролиза пептидных связей. Особенности переваривания белков у детей грудного возраста, нарушения переваривания белков у детей. Гниение белков (аминокислот) в толстом кишечнике.
Переваривание белков, то есть расщепление их до отдельных аминокислот, начинается в желудке и заканчивается в тонком кишечнике. Переваривание происходит под действием желудочного, панкреатического и кишечного соков, которые содержат протеолитические ферменты (протеазы или пептидазы). Протеолитические ферменты относятся к классу гидролаз. Они катализируют гидролиз пептидных связей СО—NН белковой молекулы.
Все протеолитические ферменты можно разделить на две группы:
- экзопептидазы – катализируют разрыв концевой пептидной связи с освобождением N- или С-концевой аминокислоты;
- эндопептидазы – гидролизуют пептидные связи внутри полипептидной цепи, продуктами реакции являются пептиды с меньшей молекулярной массой.
10.1.3. Большинство протеолитических ферментов, участвующих в переваривании белков и пептидов, синтезируются и выделяются в полость пищеварительного тракта в виде неактивных предшественников – проферментов (зимогенов). Поэтому не происходит переваривания белков клеток, вырабатывающих проферменты. Активация проферментов осуществляется в просвете желудочно-кишечного тракта путём частичного протеолиза – отщепления части пептидной цепи зимогена.
Основная масса аминокислот, образовавшихся в пищеварительном тракте в результате переваривания белков, всасывается в кровь и пополняет аминокислотный фонд организма. Определённое количество невсосавшихся аминокислот подвергается гниению в толстом кишечнике.
Гниение – превращения аминокислот, вызванные деятельностью микроорганизмов в толстом кишечнике. Усилению процессов гниения аминокислот могут способствовать:
- избыточное поступление белков с пищей;
- врождённые и приобретённые нарушения процесса всасывания аминокислот в кишечнике;
- снижение моторной функции кишечника.
В результате гниения аминокислот образуются различные вещества, многие из которых являются токсичными для организма. Некоторые примеры продуктов гниения приводятся в таблице 10.2.
Таблица 10.2
Продукты гниения аминокислот в кишечнике.
|
Аминокислоты |
Продукты гниения |
|
|
Тирозин |
Крезол |
|
|
Фенол |
||
|
Триптофан |
Скатол |
|
|
Индол |
||
|
Цистеин, |
Метилмеркаптан |
|
|
Сероводород |
||
|
Лизин |
Кадаверин |
|
|
Орнитин |
Путресцин |
|
10.2.2. Продукты гниения аминокислот являются ксенобиотиками – веществами, чужеродными для организма человека и должны быть обезврежены (инактивированы).
19. Роль липидов в организме. Пищевые липиды, суточная потребность у детей разного возраста. Особенности использования липидов в различных тканях. Бурая жировая ткань. Депонирование и мобилизация жиров в жировой ткани. Ожирение.
В состав пищевых жиров входят в, основном, триацилглицеролы (98%), фосфолипиды и холестерол. Триацилглицеролы животного происхождения содержат много насыщенных жирных кислот и имеют твёрдую консистенцию. Растительные жиры содержат больше ненасыщенных жирных кислот и имеют жидкую консистенцию (масла).
Биологическая роль: 1. являются одним из основных источников энергии; 2. служат источником незаменимых полиненасыщенных жирных кислот; 3. способствуют всасыванию из кишечника жирорастворимых витаминов. Полиненасыщенные жирные кислоты необходимы организму для построения фосфолипидов, формирующих основу всех мембранных структур клетки и липопротеинов крови. Кроме того, линолевая кислота используется для синтеза арахидоновой кислоты, служащей предшественником простагландинов, простациклинов, тромбоксанов и лейкотриенов.
Суточная потребность: 90-100 г, из них 30% должны приходиться на растительные масла. Пищевая ценность растительных жиров выше, чем животных, так как при равном энергетическом эффекте - 9 ккал на 1 г, они содержат больше незаменимых жирных кислот.
11.3.2. Нарушение соотношения доли растительных и животных жиров в рационе приводит к изменению соотношения в крови различных классов липопротеинов и, как следствие, к ишемической болезни сердца и атеросклерозу.
20. Переваривание жиров. Липазы и фосфолипазы. Желчные кислоты и парные желчные кислоты: строение, образование, биологическая роль. Особенности переваривания липидов у детей. Нарушения переваривания липидов.
Основным местом переваривания липидов является верхний отдел тонкого кишечника. Для переваривания липидов необходимы следующие условия:
- наличие липолитических ферментов;
- условия для эмульгирования липидов;
- оптимальные значения рН среды (в пределах 5,5 – 7,5).
10.3.2. В расщеплении липидов участвуют различные ферменты. Пищевые жиры у взрослого человека расщепляются в основном панкреатической липазой; обнаруживается также липаза в кишечном соке, в слюне, у грудных детей активна липаза в желудке. Липазы относятся к классу гидролаз, они гидролизуют сложноэфирные связи -О-СО- с образованием свободных жирных кислот, диацилглицеролов, моноацилглицеролов, глицерола
Поступающие с пищей глицерофосфолипиды подвергаются воздействию специфических гидролаз – фосфолипаз, расщепляющих сложноэфирные связи между компонентами фосфолипидов. Специфичность действия фосфолипаз показана на рисунке 10.4.
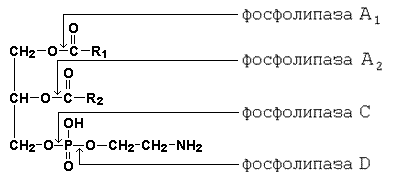
Рисунок 10.4. Специфичность действия ферментов, расщепляющих фосфолипиды.
Продуктами гидролиза фосфолипидов являются жирные кислоты, глицерол, неорганический фосфат, азотистые основания (холин, этаноламин, серин).
Пищевые эфиры холестерола гидролизуются панкреатической холестеролэстеразой с образованием холестерола и жирных кислот.
10.3.3. Уясните особенности структуры желчных кислот и их роль в переваривании жиров. Желчные кислоты – конечный продукт обмена холестерола, образуются в печени. К ним относятся: холевая (3,7,12-триоксихолановая), хенодезоксихолевая (3,7-диоксихолановая)и дезоксихолевая (3, 12-диоксихолановая) кислоты (рисунок 10.5, а). Две первые являются первичными желчными кислотами (образуются непосредственно в гепатоцитах), дезоксихолевая – вторичной (так как образуется из первичных желчных кислот под влиянием микрофлоры кишечника).
В желчи эти кислоты присутствуют в конъюгированной форме, т.е. в виде соединений с глицином Н2N-СН2-СООН или таурином Н2N-СН2-СН2-SO3H (рисунок 10.5, б).
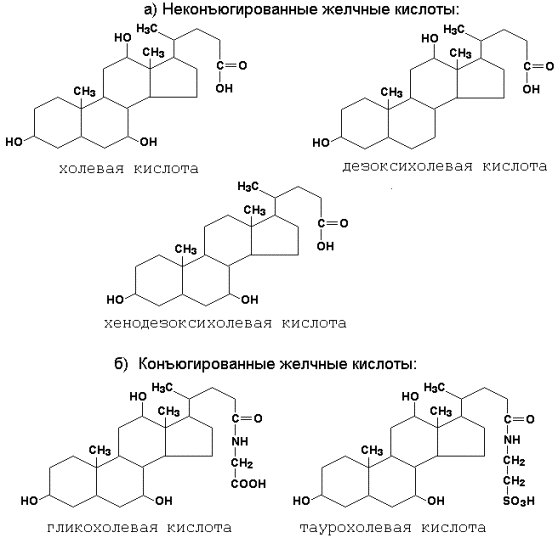
Рисунок 10.5. Строение неконъюгированных (а) и конъюгированных (б) желчных кислот.
15.1.4. Желчные кислоты обладают амфифильными свойствами: гидроксильные группы и боковая цепь гидрофильны, циклическая структура гидрофобна. Эти свойства обусловливают участие желчных кислот в переваривании липидов:
1) желчные кислоты способны эмульгировать жиры, их молекулы своей неполярной частью адсорбируются на поверхности жировых капель, в то же время гидрофильные группы вступают во взаимодействие с окружающей водной средой. В результате снижается поверхностное натяжение на границе раздела липидной и водной фаз, вследствие чего крупные жировые капли разбиваются на более мелкие;
2) желчные кислоты наряду с колипазой желчи участвуют в активировании панкреатической липазы, сдвигая её оптимум рН в кислую сторону;
3) желчные кислоты образуют с гидрофобными продуктами переваривания жиров водорастворимые комплексы, что способствует их всасыванию в стенку тонкого кишечника.
Желчные кислоты, проникающие в процессе всасывания вместе с продуктами гидролиза в энтероциты, через портальную систему поступают в печень. Эти кислоты могут повторно секретироваться с желчью в кишечник и участвовать в процессах переваривания и всасывания. Такая энтеро-гепатическая циркуляция желчных кислот может осуществляться до 10 и более раз в сутки.
ОБНОВЛЕНИЯ
ПОДПИСАТЬСЯ НА РАССЫЛКУ
ПРЕДМЕТЫ
- Анатомия
- Акушерство и гинекология
- БЖД, медицина катастроф
- Биохимия
- Биология
- Гистология
- Гигиена
- Генетика
- Диетология
- Дерматовенерология
- Инфекционные болезни
- Культурология
- Лабораторная диагностика
- Летняя практика
- Лучевая диагностика
- Медицинская информатика
- Микробиология
- Неврология
- Общественное здоровье
- Общий уход
О НАС
«Dendrit» - информационный портал для медицинских работников, студентов медицинских ВУЗов, исследователей и пациентов.
Ваш источник новостей и знаний о здоровье.