ПОДПИСАТЬСЯ НА РАССЫЛКУ
Некроз. Апоптоз.
Некроз (от греч. nekros – мертвый) – омертвение, гибель клеток и тканей в живом организме под воздействием болезнетворных факторов. Этот вид гибели клеток генетически не контролируется.
Факторы, вызывающие некроз:
ü физические (огнестрельное ранение, радиация, электричество, низкие и высокие температуры – отморожение и ожог);
ü токсические (кислоты, щелочи, соли тяжелых металлов, ферменты, лекарственные препараты, этиловый спирт и др.);
ü биологические (бактерии, вирусы, простейшие и др.);
ü аллергические (эндо- и экзоантигены, например, фибриноидный некроз при инфекционно-аллергических и аутоиммунных заболеваниях, феномен Артюса);
ü сосудистый (инфаркт – сосудистый некроз);
ü трофоневротический (пролежни, незаживающие язвы).
В зависимости от механизма действия патогенного фактора различают:
- прямой некроз, обусловленный непосредственным действием фактора (травматические, токсические и биологические некрозы);
- непрямой некроз, возникающий опосредованно через сосудистую и нервно-эндокринную системы (аллергические, сосудистые и трофоневротические некрозы).
Морфологические признаки некроза
Некрозу предшествует период некробиоза, морфологическим субстратом которого являются дистрофические изменения.
Изменения в ядрах.
Хроматин мертвой клетки конденсируется в крупные глыбки. Ядро уменьшается в объеме, становится сморщенным, плотным, интенсивно базофильным, то есть, окрашивается в темно-синий цвет гематоксилином. Этот процесс назван кариопикнозом (сморщиванием). Пикнотическое ядро может затем разрываться на многочисленные маленькие базофильные частицы (кариорексис) или подвергнуться лизису (растворению) в результате действия лизосомной дезоксирибонуклеазы (кариолизис). Тогда оно увеличивается в объеме, слабо окрашивается гематоксилином, постепенно теряются контуры ядра. При быстро развивающемся некрозе ядро подвергается лизису без пикнотической стадии.
Цитоплазматические изменения.
- цитоплазма клетки становится гомогенной и выражено ацидофильной в результате коагуляции цитоплазматических белков и разрушения (исчезновения) рибосом.
- набухание митохондрий и деструкция (разрушение) мембран органелл вызывают вакуолизацию цитоплазмы.
- переваривание клетки ферментами, которые высвобождаются из собственных лизосом, вызывает лизис клетки (аутолиз).
Таким образом, в цитоплазме происходит коагуляция белков, сменяемая обычно их колликвацией.
Изменения межклеточного вещества охватывают как межуточное вещество, так и волокнистые структуры. Чаще всего развиваются изменения, характерные для фибриноидного некроза: коллагеновые, эластические и ретикулиновые волокна превращаются в плотные, гомогенные розовые, иногда базофильные массы, которые могут подвергаться фрагментации, глыбчатому распаду либо лизироваться. Реже может наблюдаться отек, лизис и ослизнение волокнистых структур, что свойственно колликвационному некрозу.
Клинико-морфологические формы некроза
Различают коагуляционный (сухой) некроз и колликвационный (влажный) некроз.
А. Коагуляционный (сухой) некроз.
Коагуляционный некроз обычно происходит в органах, богатых белками и бедных жидкостями, например, в почках, миокарде, надпочечниках, селезенке, обычно в результате недостаточного кровообращения и аноксии, действия физических, химических и других повреждающих факторов, например, коагуляционный некроз клеток печени при вирусном поражении или при действии токсических агентов бактериального и небактериального генеза. Коагуляционный некроз еще называют сухим, поскольку он характеризуется тем, что возникающие при нем мертвые участки сухие, плотные, крошащиеся, белого или желтого цвета.
К коагуляционному некрозу относят:
Инфаркт – разновидность сосудистого (ишемического) некроза внутренних органов (кроме мозга). Это самый частый вид некроза.
Инфаркт (от лат. infarcire – начинять, набивать) – это мертвый участок органа или ткани, выключенный из кровообращения в результате внезапного прекращения кровотока (ишемии). Инфаркт – разновидность сосудистого (ишемического) коагуляционного либо колликвационного некроза. Это самый частый вид некроза.
Некрозу подвергаются как паренхиматозные клетки, так и интерстициальная ткань. Наиболее часто инфаркт возникает при тромбозе или эмболии, спазме, сдавлении артериальных сосудов. Очень редко причиной инфаркта может быть нарушение венозного оттока.
Причины развития инфаркта:
- острая ишемия, обусловленная длительным спазмом, тромбозом или эмболией, сдавлением артерии;
- функциональное напряжение органа в условиях недостаточного его кровоснабжения. Огромное значение для возникновения инфаркта имеет недостаточность анастомозов и коллатералей, которая зависит от степени поражения стенок артерий и сужения их просветов (атеросклероз, облитерирующий эндартериит), от степени нарушения кровообращения (например, венозного застоя) и от уровня выключения артерии тромбом или эмболом.
Поэтому инфаркты возникают обычно при тех заболеваниях, для которых характерны тяжелые изменения стенок артерий и общие расстройства кровообращения. Это:
- ревматические болезни;
- пороки сердца;
- атеросклероз;
- гипертоническая болезнь;
- бактериальный (инфекционный) эндокардит.
Морфология инфарктов
Макроскопическая картина инфарктов. Форма, величина, цвет и консистенция инфаркта могут быть различными.
Форма инфаркта. Обычно инфаркты имеют клиновидную форму. При этом заостренная часть клина обращена к воротам органа, а широкая часть выходит на периферию, например, под капсулу органа, под брюшину (инфаркты селезенки), под плевру (инфаркты легких) и т.д. Характерная форма инфарктов в почках, селезенке, легких определяется характером ангиоархитектоники этих органов – магистральным (симметричным дихотомическим) типом ветвления артерий. Реже инфаркты имеют неправильную форму. Такие инфаркты встречаются в сердце, мозге, кишечнике, поскольку в этих органах преобладает не магистральный, а рассыпной или смешанный тип ветвления артерий.
Величина инфарктов. Инфаркт может охватывать большую часть или весь орган (субтотальный или тотальный инфаркт) или обнаруживаться лишь под микроскопом (микроинфаркт).
Цвет и консистенция инфарктов. Если инфаркт развивается по типу коагуляционного некроза, то ткань в области омертвения уплотняется, становится суховатой, бело-желтого цвета (инфаркт миокарда, почек, селезенки). Если инфаркт образуется по типу колликвационного некроза, то мертвая ткань размягчается и разжижается (инфаркт мозга или очаг серого размягчения).
В зависимости от механизма развития и внешнего вида различают:
- белый (ишемический) инфаркт;
- красный (геморрагический) инфаркт;
- белый инфаркт с геморрагическим венчиком.
Белый (ишемический) инфаркт возникает в результате полного прекращения притока артериальной крови в органах, например, в сердце, почках, селезенке, головном мозге выше виллизиева круга. Обычно он возникает в участках с одной системой притока крови (магистральным типом ветвления артерий), в которых коллатеральное кровообращение развито слабо. Благодаря ненарушенному венозному оттоку из ишемизированной ткани и вследствие спазма дистального участка артерий после прекращения кровотока наблюдается бледность этих инфарктов. Белый (ишемический) инфаркт представляет собой участок, четко отграниченный от окружающих тканей, бело-желтого цвета, бесструктурный.
Белый инфаркт с геморрагическим венчиком представлен участком бело-желтого цвета, но этот участок окружен зоной кровоизлияний. Она образуется в результате того, что спазм сосудов по периферии инфаркта сменяется паретическим их расширением и развитием кровоизлияний. Такой инфаркт может возникать в почках, миокарде.
Красный (геморрагический) инфаркт характеризуется тем, что участок омертвения пропитан кровью, он темно-красный и хорошо отграничен. Инфаркт становится красным из-за выхода в зоне инфаркта крови из некротизированных сосудов микроциркуляторного русла. Для развития красного инфаркта имеют значение особенности ангиоархитектоники органа – две и более системы притока крови, развитость коллатералей: в легких – наличие анастомозов между бронхиальной и легочной артериями, в кишечнике – обилие анастомозов между ветвями брыжеечных артерий, в головном мозге в области виллизиева круга анастомозы между внутренними сонными и ветвями базилярной артерий. Красные инфаркты могут также возникать в ткани при растворении или фрагментации (распаде) обтурирующего тромба, что возобновляет артериальный кровоток в зоне инфаркта.
Геморрагический инфаркт редко встречается в почках и сердце. Необходимым условием для такого геморрагического пропитывания является венозный застой.
Венозный инфаркт возникает при окклюзии всей венозной дренажной системы ткани (например, тромбоз верхнего сагиттального синуса, тромбоз почечной вены, тромбоз верхней брыжеечной вены). При этом возникают тяжелый отек, застой, кровоизлияния и прогрессивное увеличение гидростатического давления в тканях. При сильном увеличении гидростатического давления затрудяется приток артериальной крови в ткань, что ведет к ишемии и инфаркту. Венозные инфаркты всегда геморрагические.
Микроскопически мертвый участок отличается потерей структуры, контуров клеток и исчезновением ядер.
Наибольшее клиническое значение имеют инфаркты сердца (миокарда), головного мозга, кишечника, легких, почек, селезенки.
В сердце инфаркт обычно белый с геморрагическим венчиком, имеет неправильную форму, встречается чаще в левом желудочке и межжелудочковой перегородке, крайне редко – в правом желудочке и предсердиях. Омертвение может локализоваться под эндокардом (субэндокардиальный инфаркт), эпикардом (субэпикардиальный инфаркт), в толще миокарда (интрамуральный) или охватывать всю толщу миокарда (трансмуральный инфаркт). В области инфаркта на эндокарде нередко образуются тромботические, а на перикарде – фибринозные наложения, что связано с развитием реактивного воспаления вокруг участков некроза. Чаще всего инфаркт миокарда встречается на фоне атеросклероза и гипертонической болезни с присоединением спазма или тромбоза артерий, являясь острой формой ишемической болезни сердца.
В головном мозге выше виллизиева круга возникает белый инфаркт, который быстро размягчается (очаг серого размягчения мозга). Если инфаркт образуется на фоне значительных расстройств кровообращения, венозного застоя, то очаг омертвения мозга пропитывается кровью и становится красным (очаг красного размягчения мозга). В области ствола мозга, ниже виллизиева круга также развивается красный инфаркт. Инфаркт локализуется обычно в подкорковых узлах, разрушая проводящие пути мозга, что проявляется параличами. Инфаркт мозга, как и инфаркт миокарда, чаще всего встречается на фоне атеросклероза и гипертонической болезни и является одним из проявлений цереброваскулярных заболеваний.
В легких в подавляющем большинстве случаев образуется геморрагический инфаркт. Причиной его чаще служит тромбоэмболия, реже – тромбоз при васкулите. Участок инфаркта хорошо отграничен, имеет форму конуса, основание которого обращено к плевре. На плевре в области инфаркта появляются наложения фибрина (реактивный плеврит). У острия конуса, обращенного к корню легкого, нередко обнаруживается тромб или эмбол в ветви легочной артерии. Омертвевшая ткань плотна, зерниста, темно-красного цвета. Геморрагический инфаркт легких обычно возникает на фоне венозного застоя, причем развитие его в значительной мере определяется особенностями ангиоархитектоники легких, наличием анастомозов между системами легочной и бронхиальных артерий. В условиях застойного полнокровия и закрытия просвета ветви легочной артерии в область омертвения ткани легкого из бронхиальной артерии поступает кровь, которая разрывает капилляры и изливается в просвет альвеол. Вокруг инфаркта нередко развивается воспаление легочной ткани (периинфарктная пневмония). Массивный геморрагический инфаркт легкого может быть причиной надпеченочной желтухи. Белый инфаркт в легких – исключительная редкость. Возникает он при склерозе и облитерации просвета бронхиальных артерий.
В почках инфаркт, как правило, белый с геморрагическим венчиком, конусовидный участок некроза охватывает либо корковое вещество, либо всю толщу паренхимы. При закрытии основного артериального ствола развивается тотальный или субтотальный инфаркт почки. Своеобразной разновидностью инфарктов являются симметричные некрозы коркового вещества почек, ведущие к развитию острой почечной недостаточности. Развитие ишемических инфарктов почек связано обычно с тромбоэмболией, реже – с тромбозом ветвей почечной артерии при ревматизме, бактериальном эндокардите, гипертонической болезни, ишемической болезни сердца. Редко при тромбозе почечных вен возникает венозный инфаркт почек.
В селезенке встречаются белые инфаркты, нередко с реактивным фибринозным воспалением капсулы и последующим образование спаек с диафрагмой, париетальным листком брюшины, петлями кишечника Ишемические инфаркты селезенки связаны с тромбозом и эмболией. При тромбозе селезеночной вены иногда, очень редко, образуются венозные инфаркты.
В кишечнике инфаркты геморрагические и всегда подвергаются септическому распаду, что ведет к прободению стенки кишки и развитию перитонита. Причиной, чаще всего, служит заворот, инвагинация кишечника, ущемленная грыжа, реже – атеросклероз с присоединением тромбоза.
Казеозный (творожистый) некроз развивается и при туберкулезе, сифилисе, лепре, а также при лимфогрануломатозе. Его еще называют специфическим, поскольку чаще всего встречается при специфических инфекционных гранулемах. Во внутренних органах выявляется сухой, крошащийся ограниченный участок ткани беловато-желтого цвета. В сифилитических гранулемах очень часто такие участки не крошащиеся, а пастообразные, напоминают аравийский клей. Это смешанный (то есть экстра- и интрацеллюлярный) тип некроза, при котором одновременно гибнет и паренхима, и строма (и клетки, и волокна). Микроскопически такой участок ткани выглядит как бесструктурный, гомогенный, окрашен гематоксилином и эозином в розовый цвет, хорошо видны глыбки хроматина ядер (кариорексис).
Восковидный, или ценкеровский некроз (некроз мышц, чаще передней брюшной стенки и бедра, при тяжелых инфекциях - брюшном и сыпном тифах, холере);
Фибриноидный некроз – тип некроза соединительной ткани. Наблюдается при аллергических и аутоиммунных болезнях (например, ревматизме, ревматоидном артрите и системной красной волчанке). Повреждаются коллагеновые волокна и гладкая мускулатура средней оболочки кровеносных сосудов. Фибриноидный некроз артериол наблюдается при злокачественной гипертензии. Этот некроз характеризуется потерей нормальной структуры коллагеновых волокон и накоплением гомогенного, ярко-розового некротического материала, который похож микроскопически на фибрин.
Жировой некроз.
Ферментный жировой некроз: жировой некроз наиболее часто происходит при остром панкреатите и повреждениях поджелудочной железы, когда панкреатические ферменты выходят из протоков в окружающие ткани. При этом в жировой ткани, окружающей поджелудочную железу, появляются непрозрачные, белые (как мел) бляшки и узелки (стеатонекроз).
Неферментный жировой некроз: неферментный жировой некроз наблюдается в молочной железе, подкожной жировой ткани и в брюшной полости. Большинство пациентов имеют в анамнезе травмы. Неферментный жировой некроз вызывает воспалительный ответ, характеризуемый наличием многочисленных макрофагов с пенистой цитоплазмой, нейтрофилов и лимфоцитов. Затем следует фиброзирование, при этом данный процесс бывает трудно отличить от опухоли.
Гангрена (от греч. gangraina – пожар): это некроз тканей, сообщающихся с внешней средой и изменяющихся под ее воздействием. Различают сухую, влажную, газовую гангрены и пролежни.
Сухая гангрена – это некроз тканей, соприкасающихся с внешней средой, протекающий без участия микроорганизмов. Сухая гангрена наиболее часто возникает на конечностях в результате ишемического коагуляционного некроза тканей. Некротизированные ткани кажутся черными, сухими, они четко отграничены от смежной жизнеспособной ткани. На границе со здоровыми тканями возникает демаркационное воспаление. Изменение цвета обусловлено превращением гемоглобиногенных пигментов в присутствии сероводорода в сульфид железа. Примерами может служить сухая гангрена:
- конечности при атеросклерозе и тромбозе ее артерий (атеросклеротическая гангрена), облитерирующем эндартериите;
- при отморожении или ожоге;
- пальцев при болезни Рейно или вибрационной болезни;
- кожи при сыпном тифе и др. инфекциях.
Влажная гангрена: развивается в результате наслоения на некротические изменения ткани тяжелой бактериальной инфекции. Под действием ферментов микроорганизмов возникает вторичная колликвация. Влажная гангрена развивается обычно в тканях, богатых влагой. Она может встречаться на конечностях, но чаще – во внутренних органах, например, в кишечнике при непроходимости брыжеечных артерий (тромбоз, эмболия), в легких как осложнение пневмонии (грипп, корь). У ослабленных инфекционным заболеванием (чаще корью) детей может развиться влажная гангрена мягких тканей щек, промежности, которую называют номой (от греч. nome - водяной рак).
Пролежень (decubitus): как разновидность гангрены выделяют пролежни - омертвение тканей (кожа, мягкие ткани), подвергающихся длительному давлению. Пролежни чаще появляются в области крестца, остистых отростков позвонков, большого вертела бедренной кости (у лежачих больных). По своему генезу это трофоневротический некроз, так как сдавливаются сосуды и нервы, что усугубляет нарушения трофики тканей у тяжелобольных, страдающих сердечно-сосудистыми, онкологическими, инфекционными или нервными болезнями.
Б. Колликвационный (влажный) некроз
Характеризуется расплавлением мертвой ткани. Он развивается в тканях, относительно бедных белками и богатых жидкостью, где имеются благоприятные условия для гидролитических процессов. Лизис клеток происходит в результате действия собственных ферментов (аутолиз). Типичным примером влажного колликвационного некроза является очаг серого размягчения (ишемический инфаркт) головного мозга.
Исход некроза.
Благоприятные исходы некроза:
- лизис;
- организация, на месте некроза в таких случаях образуется рубец (рубец на месте инфаркта).
- инкапсуляция;
- петрификация;
- оссификация;
- образование кисты.
Неблагоприятные исходы некроза:
- гнойное (септическое) расплавление очага омертвения;
- секвестрация - это формирование участка мертвой ткани, который не подвергается аутолизу и организации. Секвестры обычно возникают в костях при воспалении костного мозга - остеомиелите. Вокруг такого секвестра образуется секвестральная капсула и полость, заполненная гноем;
- мутиляция - отторжение некротизированных тканей.
Апоптоз, или запрограммированная смерть клетки, представляет собой процесс, посредством которого внутренние или внешние факторы, активируя генетическую программу, приводят к гибели клетки и ее эффективному удалению из ткани. Морфологически апоптоз проявляется гибелью единичных, беспорядочно расположенных клеток, что сопровождается формированием округлых, окруженных мембраной телец (“апоптотические тельца”), которые тут же фагоцитируются окружающими клетками.
Это энергозависимый процесс, посредством которого удаляются нежелательные и дефектные клетки организма. Он играет большую роль в морфогенезе и является механизмом постоянного контроля размеров органов. При снижении апоптоза происходит накопление клеток, пример – опухолевый рост. При увеличении апоптоза наблюдается прогрессивное уменьшение количества клеток в ткани, пример – атрофия.
Морфологические проявления апоптоза
Апоптотические клетки выглядят как округлые или овальные скопления интенсивно эозинофильной цитоплазмы с плотными фрагментами ядерного хроматина. Поскольку сжатие клетки и формирование апоптотических телец происходит быстро и также быстро они фагоцитируются, распадаются или выбрасываются в просвет органа, то на гистологических препаратах он обнаруживается в случаях его значительной выраженности. К тому же апоптоз – в отличие от некроза – никогда не сопровождается воспалительной реакцией, что также затрудняет его гистологическое выявление.
Сравнительная характеристика некроза и апоптоза
|
Признак |
Апоптоз |
Некроз |
|
Индукция |
Активируется физиологическими или патологическими стимулами |
Различная в зависимости от повреждающего фактора |
|
Распространенность |
Одиночная клетка |
Группа клеток |
|
Биохимические изменения |
Энергозависимая фрагментация ДНК эндогенными эндонуклеазами. |
Нарушение или прекращение ионного обмена. |
|
Распад ДНК |
Внутриядерная конденсация с расщеплением на фрагменты |
Диффузная локализация в некротизированной клетке |
|
Целостность клеточной мембраны |
Сохранена |
Нарушена |
|
Морфология |
Сморщивание клеток и фрагментация с формированием апоптотических телец с уплотненным хроматином |
Набухание и лизис клеток |
|
Воспалительный ответ |
Нет |
Обычно есть |
|
Удаление погибших клеток |
Поглощение (фагоцитоз) соседними клетками |
Фагоцитоз нейтрофилами и макрофагами |
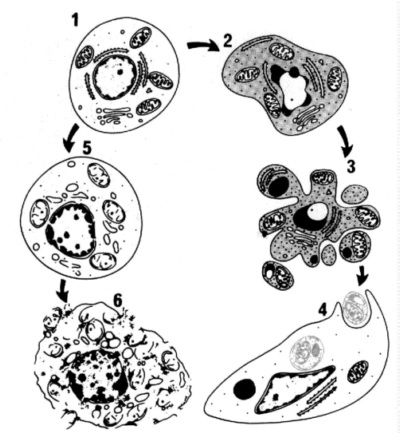
Рис. 1. Последовательность ультраструктурных изменений при апоптозе (справа) и некрозе (слева)
1 – нормальная клетка; 2 – начало апоптоза; 3 – фрагментация апоптотической клетки; 4 – фагоцитоз апоптотических телец окружающими клетками; 5 – гибель внутриклеточных структур при некрозе; 6 – разрушение клеточной мембраны.
Апоптоз принимает участие в следующих физиологических и патологических процессах:
ü запрограммированном разрушении клеток во время эмбриогенеза (включая имплантацию, органогенез);
ü гормон-зависимой инволюции органов у взрослых, например, отторжение эндометрия во время менструального цикла, атрезии фолликулов в яичниках в менопаузе и регрессия молочной железы после прекращения лактации;
ü удалении некоторых клеток при пролиферации клеточной популяции;
ü гибели отдельных клеток в опухолях, в основном при ее регрессии, но также и в активно растущей опухоли;
ü гибели клеток иммунной системы, как В-, так и Т-лимфоцитов, после истощения запасов цитокинов, а также гибели аутореактивных Т-клеток при развитии в тимусе;
ü патологической атрофии паренхиматозных органов после обтурации выводных протоков, что наблюдается в поджелудочной и слюнных железах, почках;
ü гибели клеток, вызванных действием цитотоксических Т-клеток, например, при отторжении трансплантата и болезни “трансплантат против хозяина”;
ü повреждении клеток при некоторых вирусных заболеваниях, например, при вирусном гепатите, когда фрагменты апоптотических клеток обнаруживаются в печени, как тельца Каунсильмана.
Регуляция апоптоза
Апоптоз это генетически контролируемая смерть клетки. В настоящее время выявлено большое число генов, которые кодируют вещества, необходимые для регуляции апоптоза.
Апоптоз может регулироваться:
- внешними факторами,
- автономными механизмами.
ОБНОВЛЕНИЯ
ПОДПИСАТЬСЯ НА РАССЫЛКУ
ПРЕДМЕТЫ
- Анатомия
- Акушерство и гинекология
- БЖД, медицина катастроф
- Биохимия
- Биология
- Гистология
- Гигиена
- Генетика
- Диетология
- Дерматовенерология
- Инфекционные болезни
- Культурология
- Лабораторная диагностика
- Летняя практика
- Лучевая диагностика
- Медицинская информатика
- Микробиология
- Неврология
- Общественное здоровье
- Общий уход
О НАС
«Dendrit» - информационный портал для медицинских работников, студентов медицинских ВУЗов, исследователей и пациентов.
Ваш источник новостей и знаний о здоровье.