ПОДПИСАТЬСЯ НА РАССЫЛКУ
Биохимия крови. Плазма крови. Метаболизм эритроцитов.
Тема: «БИОХИМИЯ КРОВИ. ПЛАЗМА КРОВИ: КОМПОНЕНТЫ И ИХ ФУНКЦИИ. МЕТАБОЛИЗМ ЭРИТРОЦИТОВ. ЗНАЧЕНИЕ БИОХИМИЧЕСКОГО АНАЛИЗА КРОВИ В КЛИНИКЕ»
1. Белки плазмы крови: биологическая роль. Содержание белковых фракций в плазме. Изменения белкового состава плазмы при патологических состояниях (гиперпротеинемия, гипопротеинемия, диспротеинемия, парапротеинемия).
2. Белки острой фазы воспаления: биологическая роль, примеры белков.
3. Липопротеиновые фракции плазмы крови: особенности состава, роль в организме.
4. Иммуноглобулины плазмы крови: основные классы, схема строения, биологические функции. Интерфероны: биологическая роль, механизм действия (схема).
5. Ферменты плазмы крови (секреторные, экскреторные, индикаторные): диагностическое значение исследования активности аминотрансфераз (АЛТ и АСТ), щелочной фосфатазы, амилазы, липазы, трипсина, изоферментов лактатдегидрогеназы, креатинкиназы.
6. Небелковые азотсодержащие компоненты крови (мочевина, аминокислоты, мочевая кислота, креатинин, индикан, прямой и непрямой билирубин): строение, биологическая роль, диагностическое значение их определения в крови. Понятие об азотемии.
7. Безазотистые органические компоненты крови (глюкоза, холестерол, свободные жирные кислоты, кетоновые тела, пируват, лактат), диагностическое значение их определения в крови.
8. Особенности строения и функции гемоглобина. Регуляторы сродства гемоглобина к О2 . Молекулярные формы гемоглобина. Производные гемоглобина. Клинико-диагностическое значение определения гемоглобина в крови.
9. Метаболизм эритроцита: роль гликолиза и пентозофосфатного пути в зрелых эритроцитах. Глутатион: роль в эритроцитах. Ферментные системы, участвующие в обезвреживании активных форм кислорода.
10. Свёртывание крови как каскад активации проферментов. Внутренний и внешний пути свёртывания. Общий путь свёртывания крови: активация протромбина, превращение фибриногена в фибрин, образование фибрина-полимера.
11. Участие витамина К в посттрансляционной модификации факторов свёртывания крови. Дикумарол как антивитамин К.
30.1. Состав и функции крови.
Кровь - жидкая подвижная ткань, циркулирующая в замкнутой системе кровеносных сосудов, транспортирующая различные химические вещества к органам и тканям, и осуществляющая интеграцию метаболических процессов, протекающих в различных клетках.
Кровь состоит из плазмы и форменных элементов (эритроцитов, лейкоцитов и тромбоцитов). Сыворотка крови отличается от плазмы отсутствием фибриногена. 90% плазмы крови составляет вода, 10% - сухой остаток, в состав которого входят белки, небелковые азотистые компоненты (остаточный азот), безазотистые органические компоненты и минеральные вещества.
30.2. Белки плазмы крови.
Плазма крови содержит сложную многокомпонентную (более 100) смесь белков, различающихся по происхождению и функциям. Большинство белков плазмы синтезируется в печени. Иммуноглобулины и ряд других защитных белков иммунокомпетентными клетками.
Содержание общего белка в сыворотке крови здорового человека составляет 65 - 85 г/л (в плазме крови этот показатель на 2 – 4 г/л выше за счёт фибриногена).
30.2.1. Белковые фракции. При помощи высаливания белков плазмы можно выделить альбуминовую и глобулиновую фракции. В норме соотношение этих фракций составляет 1,5 – 2,5. Использование метода электрофореза на бумаге позволяет выявить 5 белковых фракций (в порядке убывания скорости миграции): альбумины, α1-, α2-, β- и γ-глобулины. При использовании более тонких методов фракционирования в каждой фракции, кроме альбуминовой, можно выделить целый ряд белков (содержание и состав белковых фракций сыворотки крови см. рисунок 1).
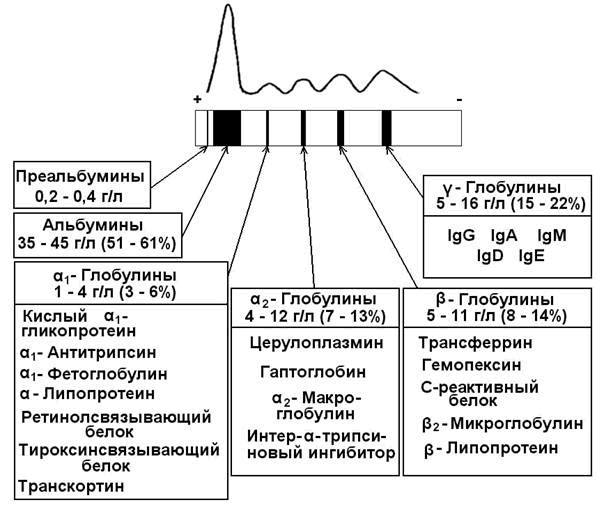
Рисунок 1. Электрофореграмма белков сыворотки крови и состав белковых фракций.
Альбумины – белки с молекулярной массой около 70000 Да. Благодаря гидрофильности и высокому содержанию в плазме играют важную роль в поддержании коллоидно-осмотического (онкотического) давления крови и регуляции обмена жидкостей между кровью и тканями. Выполняют транспортную функцию: осуществляют перенос свободных жирных кислот, желчных пигментов, стероидных гормонов, ионов Са2+, многих лекарств. Альбумины также служат богатым и быстро реализуемым резервом аминокислот.
α1-Глобулины:
- Кислый α1-гликопротеин (орозомукоид) – содержит до 40% углеводов, изоэлектрическая точка его находится в кислой среде (2,7). Функция этого белка до конца не установлена; известно, что на ранних стадиях воспалительного процесса орозомукоид способствует образованию коллагеновых волокон в очаге воспаления (Я.Мусил, 1985).
- α1-Антитрипсин – ингибитор ряда протеаз (трипсина, химотрипсина, калликреина, плазмина). Врождённое снижение содержания α1-антитрипсина в крови может быть фактором предрасположенности к бронхо-лёгочным заболеваниям, так как эластические волокна лёгочной ткани особенно чувствительны к действию протеолитических ферментов.
- Ретинолсвязывающий белок осуществляет транспорт жирорастворимого витамина А.
- Тироксинсвязывающий белок – связывает и транспортирует иодсодержащие гормоны щитовидной железы.
- Транскортин – связывает и транспортирует глюкокортикоидные го рмоны (кортизол, кортикостерон).
α2-Глобулины:
- Гаптоглобины (25% α2-глобулинов) – образуют стабильный комплекс с гемоглобином, появляющимся в плазме в результате внутрисосудистого гемолиза эритроцитов. Комплексы гаптоглобин-гемоглобин поглощаются клетками РЭС, где гем и белковые цепи подвергаются распаду, а железо повторно используется для синтеза гемоглобина. Тем самым предотвращается потеря железа организмом и повреждение почек гемоглобином.
- Церулоплазмин – белок, содержащий ионы меди (одна молекула церулоплазмина содержит 6-8 ионов Cu2+), которые придают ему голубую окраску. Является транспортной формой ионов меди в организме. Обладает оксидазной активностью: окисляет Fe2+ в Fe3+, что обеспечивает связывание железа трансферрином. Способен окислять ароматическиеамины, участвует в обмене адреналина, норадреналина, серотонина.
β-Глобулины:
- Трансферрин – главный белок β-глобулиновой фракции, участвует в связывании и транспорте трёхвалентного железа в различные ткани, особенно в кроветворные. Трансферрин регулирует содержание Fe3+ в крови, предотвращает избыточное накопление и потерю с мочой.
- Гемопексин – связывает гем и предотвращает его потерю почками. Комплекс гем-гемопексин улавливается из крови печенью.
- С-реактивный белок (С-РБ) – белок, способный преципитировать (в присутствии Са2+) С-полисахарид клеточной стенки пневмококка. Биологическая роль его определяется способностью активировать фагоцитоз и ингибировать процесс агрегации тромбоцитов. У здоровых людей концентрация С-РБ в плазме ничтожно мала и стандартными методами не определяется. При остром воспалительном процессе она увеличивается более чем в 20 раз, в этом случае С-РБ обнаруживается в крови. Исследование С-РБ имеет преимущество перед другими маркерами воспалительного процесса: определением СОЭ и подсчётом числа лейкоцитов. Данный показатель более чувствителен, его увеличение происходит раньше и после выздоровления быстрее возвращается к норме.
γ-Глобулины:
- Иммуноглобулины (IgA, IgG, IgM, IgD, IgE) представляют собой антитела, вырабатываемые организмом в ответ на введение чужеродных веществ с антигенной активностью. Подробнее об этих белках см. 1.2.5.
30.2.2. Количественные и качественные изменения белкового состава плазмы крови. При различных патологических состояниях белковый состав плазмы крови может изменяться. Основными видами изменений являются:
- Гиперпротеинемия - увеличение содержания общего белка плазмы. Причины: потеря большого количества воды (рвота, диарея, обширные ожоги), инфекционные заболевания (за счёт увеличения количества γ-глобулинов).
- Гипопротеинемия - уменьшение содержания общего белка в плазме. Наблюдается при заболеваниях печени (вследствие нарушения синтеза белков), при заболеваниях почек (вследствие потери белков с мочой), при голодании (вследствие недостатка аминокислот для синтеза белков).
- Диспротеинемия - изменение процентного соотношения белковых фракций при нормальном содержании общего белка в плазме крови, например, снижение содержания альбуминов и увеличение содержания одной или нескольких глобулиновых фракций при различных воспалительных заболеваниях.
- Парапротеинемия - появление в плазме крови патологических иммуноглобулинов - парапротеинов, отличающихся от нормальных белков по физико-химическим свойствам и биологической активности. К таким белкам относятся, например, криоглобулины, образующие друг с другом преципитаты при температуре ниже 37° С. Парапротеины обнаруживаются в крови при макроглобулинемии Вальденстрема, при миеломной болезни (в последнем случае они могут преодолевать почечный барьер и обнаруживаться в моче как белки Бенс-Джонса). Парапротеинемия, как правило, сопровождается гиперпротеинемией.
30.2.3. Липопротеиновые фракции плазмы крови. Липопротеины - сложные соединения, осуществляющие транспорт липидов в крови. В состав их входят: гидрофобное ядро, содержащее триацилглицеролы и эфиры холестерола, иамфифильная оболочка, образованная фосфолипидами, свободным холестеролом и белками-апопротеинами (рисунок 2). В плазме крови человека содержатся следующие фракции липопротеинов:
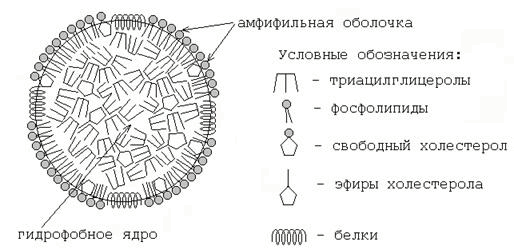
Рисунок 2. Схема строения липопротеина плазмы крови.
- Липопротеины высокой плотности или α-липопротеины, так как при электрофорезе на бумаге они движутся вместе с α-глобулинами. Содержат много белков и фосфолипидов, транспортируют холестерол из периферических тканей в печень.
- Липопротеины низкой плотности или β-липопротеины, так как при электрофорезе на бумаге они движутся вместе с β-глобулинами. Богаты холестеролом; транспортируют его из печени в периферические ткани.
- Липопротеины очень низкой плотности или пре-β-липопротеины (на электрофореграмме расположены между α- и β-глобулинами). Служат транспортной формой эндогенных триацилглицеролов, являются предшественниками липопротеинов низкой плотности.
- Хиломикроны - электрофоретически неподвижны; в крови, взятой натощак, отсутствуют. Являются транспортной формой экзогенных (пищевых) триацилглицеролов.
30.2.4. Белки острой фазы воспаления. Это белки, содержание которых увеличивается в плазме крови при остром воспалительном процессе. К ним относятся, например, следующие белки:
- гаптоглобин;
- церулоплазмин;
- С-реактивный белок;
- α1-антитрипсин;
- фибриноген (компонент свёртывающей системы крови; см. 30.7.2).
Скорость синтеза этих белков увеличивается прежде всего за счёт снижения образования альбуминов, трансферрина и альбуминов (небольшая фракция белков плазмы, обладающая наибольшей подвижностью при диск-электрофорезе, и которой соответствует полоса на электрофореграмме перед альбуминами), концентрация которых при остром воспалении снижается.
Биологическая роль белков острой фазы: а) все эти белки являются ингибиторами ферментов, освобождаемых при разрушении клеток, и предупреждают вторичное повреждение тканей; б) эти белки обладают иммунодепрессорным действием (В.Л.Доценко, 1985).
30.2.5. Защитные белки плазмы крови. К белкам, выполняющим защитную функцию, относятся иммуноглобулины и интерфероны.
Иммуноглобулины (антитела) - группа белков, вырабатываемых в ответ на попадание в организм чужеродных структур (антигенов). Они синтезируются в лимфоузлах и селезёнке лимфоцитами В. Выделяют 5 классов иммуноглобулинов - IgA, IgG, IgM, IgD, IgE.
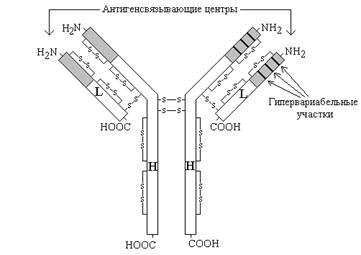
Рисунок 3. Схема строения иммуноглобулинов (серым цветом показана вариабельная область, не закрашена - константная область).
Молекулы иммуноглобулинов имеют единый план строения. Структурную единицу иммуноглобулина (мономер) образуют четыре полипептидные цепи, соединённые между собой дисульфидными связями: две тяжёлые (цепи Н) и две лёгкие (цепи L) (см. рисунок 3). IgG, IgD и IgЕ по своей структуре, как правило, являются мономерами, молекулы IgM построены из пяти мономеров, IgA состоят из двух и более структурных единиц, или являются мономерами.
Белковые цепи, входящие в состав иммуноглобулинов, можно условно разделить на специфические домены, или области, имеющие определённые структурные и функциональные особенности.
N-концевые участки как L-, так и Н-цепей называются вариабельной областью (V), так как их структура характеризуется существенными различиями у разных классов антител. Внутри вариабельного домена имеются 3 гипервариабельных участка, отличающихся наибольшим разнообразием аминокислотной последовательности. Именно вариабельная область антител ответственна за связывание антигенов по принципу комплементарности; первичная структура белковых цепей в этой области определяет специфичность антител.
С-концевые домены Н- и L-цепей обладают относительно постоянной первичной структурой в пределах каждого класса антител и называются константной областью (С). Константная область определяет свойства различных классов иммуноглобулинов, их распределение в организме, может принимать участие в запуске механизмов, вызывающих уничтожение антигенов.
Интерфероны - семейство белков, синтезируемых клетками организма в ответ на вирусную инфекцию и обладающих противовирусным эффектом. Различают несколько типов интерферонов, обладающих специфическим спектром действия: лейкоцитарный (α-интерферон), фибробластный (β-интерферон) и& иммунный (γ-интерферон). Интерфероны синтезируются и секретируются одними клетками и проявляют свой эффект, воздействуя на другие клетки, в этом отношении они подобны гормонам. Механизм действия интерферонов показан на рисунке 4.
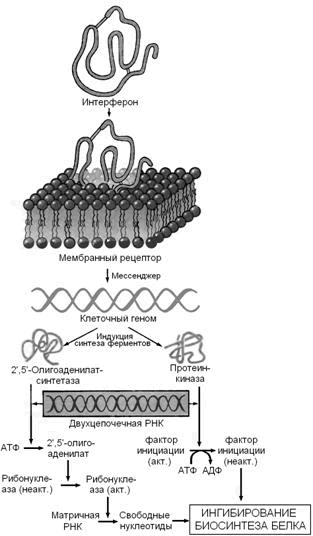
Рисунок 4. Механизм действия интерферонов (Ю.А.Овчинников, 1987).
Связываясь с клеточными рецепторами, интерфероны индуцируют синтез двух ферментов — 2',5'-олигоаденилатсинтетазы и протеинкиназы, вероятно, за счет инициации транскрипции соответствующих генов. Оба образующихся фермента проявляют свою активность в присутствии двухцепочечных РНК, а именно такие РНК являются продуктами репликации многих вирусов или содержатся в их вирионах. Первый фермент синтезирует 2',5'-олигоаденилаты (из АТФ), которые активируют клеточную рибонуклеазу I; второй фермент фосфорилирует фактор инициации трансляции IF2. Конечным результатом этих процессов является ингибирование биосинтеза белка и размножения вируса в инфицированной клетке (Ю.А.Овчинников, 1987).
30.2.6. Ферменты плазмы крови. Все ферменты, содержащиеся в плазме крови, можно разделить на три группы:
- секреторные ферменты - синтезируются в печени, выделяются в кровь, где выполняют свою функцию (например, факторы свёртывания крови);
- экскреторные ферменты - синтезируются в печени, в норме выделяются с желчью (например, щелочная фосфатаза), их содержание и активность в плазме крови возрастает при нарушении оттока желчи;
- индикаторные ферменты - синтезируются в различных тканях и попадают в кровь при разрушении клеток этих тканей. В разных клетках преобладают различные ферменты, поэтому при повреждении того или иного органа в крови появляются характерные для него ферменты. Это может быть использовано в диагностике заболеваний.
Например, при повреждении клеток печени (гепатит) в крови возрастает активность аланинаминотраноферазы (АЛТ), аспартатаминотрансферазы (ACT), изофермента лактатдегидрогеназы ЛДГ5, глутаматдегидрогеназы, орнитинкарбамоилтрансферазы.
При повреждении клеток миокарда (инфаркт) в крови возрастает активность аспартатаминотрансферазы (ACT), иэофермента лактатдегидрогеназы ЛДГ1, изофермента креатинкиназы MB.
При повреждении клеток поджелудочной железы (панкреатит) в крови возрастает активность трипсина, α-амилазы, липазы.
30.3. Небелковые азотистые компоненты крови (остаточный азот).
К этой группе веществ относятся: мочевина, мочевая кислота, аминокислоты, креатин, креатинин, аммиак, индикан, билирубин и другие соединения (см. рисунок 5). Содержание остаточного азота в плазме крови здоровых людей - 15-25 ммоль/л. Повышение содержания остаточного азота в крови называется азотемией. В зависимости от причины, азотемия подразделяется на ретенционную и продукционную.
Ретенционная азотемия возникает при нарушении выведения продуктов азотистого обмена (в первую очередь мочевины) с мочой и характерна для недостаточности функции почек. В этом случае до 90% небелкового азота крови приходится на азот мочевины вместо 50% в норме.
Продукционная азотемия развивается при избыточном поступлении азотистых веществ в кровь вследствие усиленного распада тканевых белков (длительное голодание, сахарный диабет, тяжёлые ранения и ожоги, инфекционные заболевания).
Определение остаточного азота проводят в в безбелковом фильтрате сыворотки крови. В результате минерализации безбелкового фильтрата при нагревании с концентрированной Н2SO4 азот всех небелковых соединений переходит в форму (NH4)2SO4. Ионы NH4+ определяют с помощью реактива Несслера.
- Мочевина - главный конечный продукт обмена белков в организме человека. Образуется в результате обезвреживания аммиака в печени, выводится из организма почками. Поэтому содержание мочевины в крови снижается при заболеваниях печени и возрастает при почечной недостаточности.
- Аминокислоты - поступают в кровь при всасывании из желудочно-кишечного тракта или являются продуктами распада тканевых белков. В крови здоровых людей среди аминокислот преобладают аланин и глутамин, которые наряду с участием в биосинтезе белков являются транспортными формами аммиака.
- Мочевая кислота - конечный продукт катаболизма пуриновых нуклеотидов. Содержание её в крови возрастает при подагре (в результате усиленного образования) и при нарушениях функции почек (из-за недостаточного выведения).
- Креатин - синтезируется в почках и печени, в мышцах превращается в креатинфосфат - источник энергии для процессов мышечного сокращения. При заболеваниях мышечной системы содержание креатина в крови значительно возрастает.
- Креатинин - конечный продукт азотистого обмена, образуется в результате дефосфорилирования креатинфосфата в мышцах, выводится из организма почками. Содержание креатинина в крови снижается при заболеваниях мышечной системы, повышается при почечной недостаточности.
- Индикан - продукт обезвреживания индола, образуется в печени, выводится почками. Содержание его в крови снижается при заболеваниях печени, повышается - при усилении процессов гниения белков в кишечнике, при заболеваниях почек.
- Билирубин (прямой и непрямой) - продукты катаболизма гемоглобина. Содержание билирубина в крови увеличивается при желтухах: гемолитической (за счёт непрямого билирубина), обтурационной (за счёт прямого билирубина), паренхиматозной (за счёт обеих фракций).
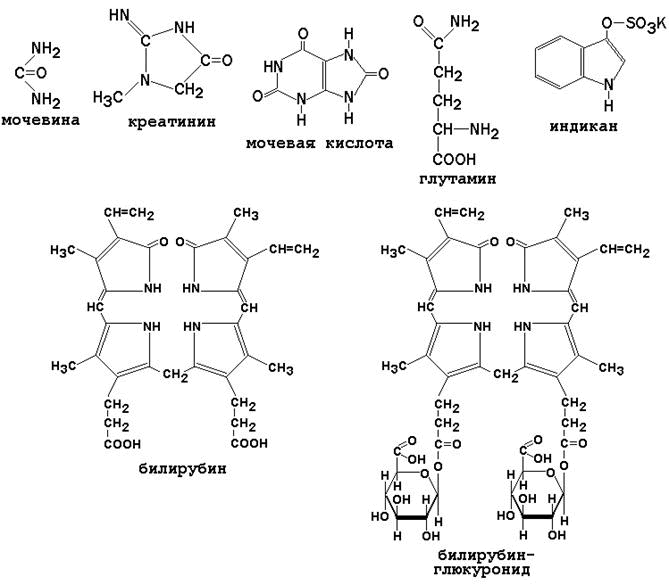
Рисунок 5. Небелковые азотистые соединения плазмы крови.
30.4. Безазотистые органические компоненты крови.
В эту группу веществ входят питательные вещества (углеводы, липиды) и продукты их метаболизма (органические кислоты). Наибольшее значение в клинике имеет определение содержания в крови глюкозы, холестерола, свободных жирных кислот, кетоновых тел и молочной кислоты. Формулы этих веществ представлены на рисунке 6.
- Глюкоза - главный энергетический субстрат организма. Содержание её у здоровых людей в крови натощак - 3,3 - 5,5 ммоль/л. Повышение содержания глюкозы в крови (гипергликемия) наблюдается после приёма пищи, при эмоциональном стрессе, у больных сахарным диабетом, гипертиреозом, болезнью Иценко-Кушинга. Снижение содержания глюкозы в крови (гипогликемия) наблюдается при голодании, интенсивных физических нагрузках, остром алкогольном отравлении, передозировке инсулина.
- Холестерол - обязательный липидный компонент биологических мембран, предшественник стероидных гормонов, витамина D3, желчных кислот. Содержание его в плазме крови здоровых людей - 3,9 - 6,5 ммоль/л. Повышение содержания холестерола в крови (гиперхолестеролемия) наблюдается при атеросклерозе, сахарном диабете, микседеме, желчно-каменной болезни. Снижение уровня холестерола в крови (гипохолестеролемия) обнаруживается при гипертиреозе, циррозе печени, заболеваниях кишечника, голодании, при приёме желчегонных препаратов.
- Свободные жирные кислоты (СЖК) используются тканями и органами в качестве энергетического материала. Содержание СЖК в крови повышается при голодании, сахарном диабете, после введения адреналина и глюкокортикоидов; снижается при гипотиреозе, после введения инсулина.
- Кетоновые тела. К кетоновым телам относятся ацетоацетат,β-гидроксибутират, ацетон - продукты неполного окисления жирных кислот. Содержание кетоновых тел в крови повышается (гиперкетонемия) при голодании, лихорадке, сахарном диабете.
- Молочная кислота (лактат) - конечный продукт анаэробного окисления углеводов. Содержание её в крови повышается при гипоксии (физические нагрузки, заболевания лёгких, сердца, крови).
- Пировиноградная кислота (пируват) – промежуточный продукт катаболизма углеводов и некоторых аминокислот. Наиболее резкое повышение содержания пировиноградной кислоты в крови отмечается при мышечной работе и недостаточности витамина В1.
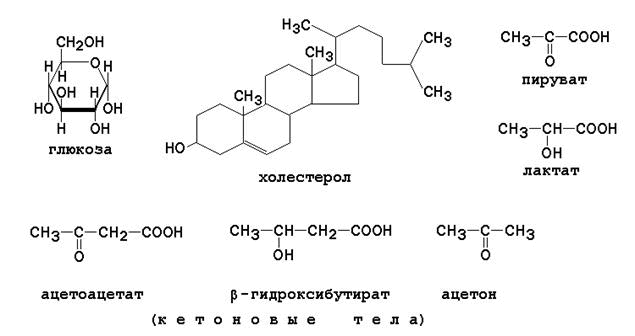
Рисунок 6. Безазотистые органические вещества плазмы крови.
30.5. Минеральные компоненты плазмы крови.
Минеральные вещества являются необходимыми компонентами плазмы крови. Важнейшими катионами являются ионы натрия, калия, кальция и магния. Им соответствуют анионы: хлориды, бикарбонаты, фосфаты, сульфаты. Часть катионов в плазме крови связаны с органическими анионами и белками. Сумма всех катионов равна сумме анионов, так как плазма крови электронейтральна.
- Натрий – основной катион внеклеточной жидкости. Его содержание в плазме крови 135 – 150 ммоль/л. Ионы натрия участвуют в поддержании осмотического давления внеклеточной жидкости. Гипернатриемия наблюдается при гиперфункции коры надпочечников, при введении гипертонического раствора хлорида натрия парентерально. Гипонатриемия может быть обусловлена бессолевой диетой, надпочечниковой недостаточностью, диабетическим ацидозом.
- Калий является основным внутриклеточным катионом. В плазме крови он содержится в количестве 3,9 ммоль/л, а в эритроцитах – 73,5 – 112 ммоль/л. Как и натрий, калий поддерживает осмотический и кислотно-основный гомеостаз в клетке. Гиперкалиемия отмечается при усиленном разрушении клеток (гемолитическая анемия, синдром длительного раздавливания), при нарушении выделения калия почками, при обезвоживании организма. Гипокалиемия наблюдается при гиперфункции коры надпочечников, при диабетическом ацидозе.
- Кальций в плазме крови содержится в виде форм. Выполняющих различные функции: связанный с белками (0,9 ммоль/л), ионизированный (1,25 ммоль/л) и неионизированный (0,35 ммоль/л). Биологически активным является только ионизированный кальций. Гиперкальциемия наблюдается при гиперпаратиреозе, гипервитаминозе D, синдроме Иценко-Кушинга, деструктивных процессах в костной ткани. Гипокальциемия встречается при рахите, гипопаратиреозе, заболеваниях почек.
- Хлориды содержатся в плазме крови в количестве 95 – 110 ммоль/л, участвуют в поддержании осмотического давления, кислотно-основного состояния внеклеточной жидкости. Гиперхлоремия наблюдается при сердечной недостаточности, артериальной гипертензии, гипохлоремия – при рвоте, заболеваниях почек.
- Фосфаты в плазме крови являются компонентами буферной системы, их концентрация составляет 1 – 1,5 ммоль/л. Гиперфосфатемия наблюдается при заболеваниях почек, гипопаратиреозе, гипервитаминозе D. Гипофосфатемия отмечена при гиперпаратиреозе, микседеме, рахите.
0.6. Кислотно-основное состояние и его регуляция.
Кислотно-основное состояние (КОС) - соотношение концентрации водородных (Н+) и гидроксильных (ОН—) ионов в жидкостях организма. Для здорового человека характерно относительное постоянство показателей КОС, обусловленное совместным действием буферных систем крови и физиологического контроля (органы дыхания и выделения).
30.6.1. Буферные системы крови. Буферные системы организма состоят из слабых кислот и их солей с сильными основаниями. Каждая буферная система характеризуется двумя показателями:
- рН буфера (зависит от соотношения компонентов буфера);
- буферная ёмкость, то есть количество сильного основания или кислоты, которое нужно прибавить к буферному раствору для изменения рН на единицу (зависит от абсолютных концентраций компонентов буфера).
Различают следующие буферные системы крови:
- бикарбонатная (H2CO3/NaHCO3);
- фосфатная (NaH2PO4/Na2HPO4);
- гемоглобиновая (дезоксигемоглобин в качестве слабой кислоты/ калиевая соль оксигемоглобина);
- белковая (действие её обусловлено амфотерностью белков). Бикарбонатная и тесно связанная с ней гемоглобиновая буферные системы составляют в совокупности более 80% буферной ёмкости крови.
30.6.2. Дыхательная регуляция КОС осуществляется путём изменения интенсивности внешнего дыхания. При накоплении в крови СО2 и Н+ усиливается лёгочная вентиляция, что приводит к нормализации газового состава крови. Снижение концентрации углекислоты и Н+ вызывает уменьшение лёгочной вентиляции и нормализацию данных показателей.
30.6.3. Почечная регуляция КОС осуществляется главным образом за счёт трёх механизмов:
- реабсорбции бикарбонатов (в клетках почечных канальцев из Н2О и СО2 образуется угольная кислота Н2СО3; она диссоциирует, Н+ выделяется в мочу, НСО3— реабсорбируетоя в кровь);
- реабсорбции Na+ из клубочкового фильтрата в обмен на Н+ (при этом Na2HPO4 в фильтрате переходит в NaH2PO4 и увеличивается кислотность мочи);
- секреции NH4+ (при гидролизе глутамина в клетках канальцев образуется NH3; он взаимодействует с H+, образуются ионы NH4+, которые выводятся с мочой.
30.6.4. Лабораторные показатели КОС крови. Для характеристики КОС используют следующие показатели:
- рН крови;
- парциальное давление СО2 (рСО2) крови;
- парциальное давление О2 (рО2) крови;
- содержание бикарбонатов в крови при данных значениях рН и рСО2 (актуальный или истинный бикарбонат, АВ);
- содержание бикарбонатов в крови пациента в стандартных условиях, т.е. при рСО2=40 мм рт.ст. (стандартный бикарбонат, SB);
- сумма оснований всех буферных систем крови (ВВ);
- избыток или дефицит оснований крови по сравнению с нормальным для данного пациента показателем (BE, от англ. base excess).
Первые три показателя определяются непосредственно в крови с помощью специальных электродов, на основании полученных данных рассчитываются остальные показатели с помощью номограмм или формул.
30.6.5. Нарушения КОС крови. Известны четыре главные формы нарушений кислотно-основного состояния:
- метаболический ацидоз - возникает при сахарном диабете и голодании (за счёт накопления кетоновых тел в крови), при гипоксии (за счёт накопления лактата). При этом нарушении снижается рСО2 и [НСО3-] крови, увеличивается экскреция NH4+ с мочой;
- дыхательный ацидоз - возникает при бронхите, пневмонии, бронхиальной астме (в результате задержки углекислоты в крови). При этом нарушении повышается рСО2 и [HCO3-] крови, увеличивается экскреция NH4+ с мочой;
- метаболический алкалоз - развивается при потере кислот, например, при неукротимой рвоте. При этом нарушении повышается рСО2 и [HCO3-] крови, увеличивается экскреция НСО3- с мочой, снижается кислотность мочи.
- дыхательный алкалоз - наблюдается при усиленной вентиляции лёгких, например, у альпинистов на большой высоте. При этом нарушении снижается рСО2 и [НСО3-] крови, уменьшается кислотность мочи.
Для лечения метаболического ацидоза используют введение раствора бикарбоната натрия; для лечения метаболического алкалоза - введение раствора глутаминовой кислоты.
30.7. Некоторые молекулярные механизмы свёртывания крови.
30.7.1. Свёртывание крови - совокупность молекулярных процессов, приводящих к прекращению кровотечения из повреждённого сосуда в результате образования кровяного сгустка (тромба). Общая схема процесса свёртывания крови представлена на рисунке 7.
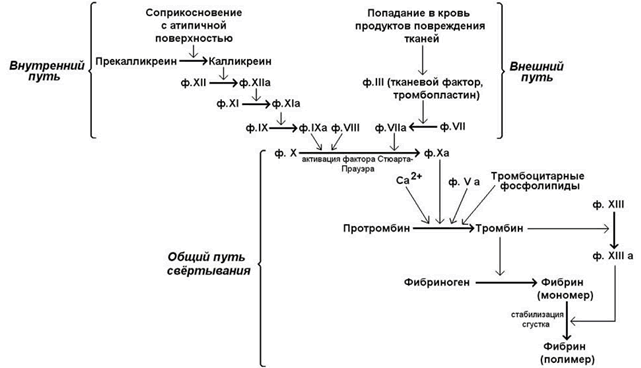
Рисунок 7. Общая схема свёртывания крови.
Большинство факторов свёртывания присутствует в крови в виде неактивных предшественников - проферментов, активация которых осуществляется путём частичного протеолиза. Ряд факторов свёртывания крови являются витамин К-зависимыми: протромбин (фактор II), проконвертин (фактор VII), факторы Кристмаса (IX) и Стюарта-Прауэра (Х). Роль витамина К определяется участием в карбоксилировании остатков глутамата в N-концевом участке этих белков с образованием γ-карбоксиглутамата.
Свёртывание крови представляет собой каскад реакций, в котором активированная форма одного фактора свёртывания катализирует активацию следующего до тех пор, пока конечный фактор, который является структурной основой тромба, не будет активирован.
Особенности каскадного механизма заключаются в следующем:
1) в отсутствие фактора, инициирующего процесс тромбообразования, реакция не может произойти. Поэтому процесс свёртывания крови будет ограничен только тем участком кровяного русла, где появляется такой инициатор;
2) факторы, действующие на начальных этапах свёртывания крови, требуются в очень малых количествах. На каждом звене каскада их эффект многократно усиливается (амплифицируется), что обеспечивает в итоге быструю ответную реакцию на повреждение.
В обычных условиях существуют внутренний и внешний пути свёртывания крови. Внутренний путь инициируется соприкосновением с атипичной поверхностью, что приводит к активации факторов, исходно присутствовавших в крови.Внешний путь свёртывания инициируется соединениями, в обычных условиях в крови не присутствующими, но поступающими туда в результате повреждения тканей. Для нормального протекания процесса свёртывания крови необходимы оба эти механизма; они различаются только на начальных этапах, а затем объединяются в общий путь, приводящий к образованию фибринового сгустка.
Далее рассматриваются только молекулярные механизмы общего пути свёртывания – активация протромбина и превращение фибриногена в фибрин-мономер и фибрин-полимер.
30.7.2. Механизм активации протромбина. Неактивный предшественник тромбина – протромбин – синтезируется в печени. В его синтезе участвует витамин К. Протромбин содержит остатки редкой аминокислоты – γ-карбоксиглутамата сокращённое обозначение – Gla). В процессе активации протромбина участвуют тромбоцитарные фосфолипиды, ионы Са2+ и факторы свёртывания Va и Хa. Механизм активации представляется следующим образом (рисунок 8).
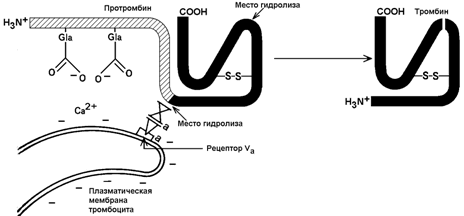
Рисунок 8. Схема активации протромбина на тромбоцитах (Р.Марри и соавт., 1993).
Повреждение кровеносного сосуда приводит к взаимодействию тромбоцитов крови с коллагеновыми волокнами сосудистой стенки. Это вызывает разрушение тромбоцитов и способствует выходу наружу отрицательно заряженных молекул фосфолипидов внутренней стороны плазматической мембраны тромбоцитов. Отрицательно заряженные группировки фосфолипидов связывают ионы Са2+. Ионы Са2+ в свою очередь взаимодействуют с остатками γ-карбоксиглутамата в молекуле протромбина. Эта молекула фиксируется на мембране тромбоцита в нужной ориентации.
Тромбоцитарная мембрана содержит также рецепторы для фактора Va. Этот фактор связывается с мембраной и присоединяет фактор Хa. Фактор Хa является протеазой; он расщепляет молекулу протромбина в определённых местах, в результате образуется активный тромбин.
30.7.3. Превращение фибриногена в фибрин. Фибриноген (фактор I) - растворимый гликопротеин плазмы с молекулярной массой около 340 000. Он синтезируется в печени. Молекула фибриногена состоит из шести полипептидных цепей: две А α-цепи, две В β-цепи, и две γ-цепи (см. рисунок 9). Концы полипептидных цепей фибриногена несут отрицательный заряд. Это обусловлено присутствием большого количества остатков глутамата и аспартата в N-концевых областях цепей Аa и Вb. Кроме того, В-области цепей Вb содержат остатки редкой аминокислоты тирозин-О-сульфата, также заряженные отрицательно:
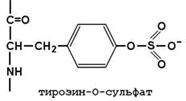
Это способствует растворимости белка в воде и препятствует агрегации его молекул.
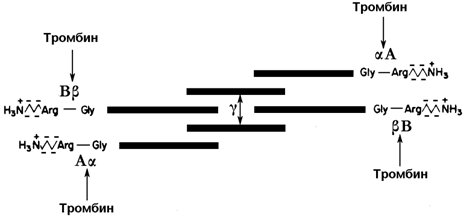
Рисунок 9. Схема строения фибриногена; стрелками показаны связи, гидролизуемые тромбином. Р.Марри и соавт., 1993).
Превращение фибриногена в фибрин катализирует тромбин (фактор IIa). Тромбин гидролизует четыре пептидные связи в фибриногене: две связи в цепях А α и две связи в цепях В β. От молекулы фибриногена отщепляются фибринопептиды А и В и образуется фибрин-мономер (его состав α2 β2 γ2). Мономеры фибрина нерастворимы в воде и легко ассоциируют друг с другом, образуя фибриновый сгусток.
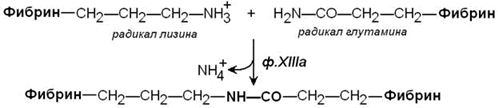
Стабилизация фибринового сгустка происходит под действием фермента трансглутаминазы (фактор XIIIa). Этот фактор также активируется тромбином. Трансглутаминаза образует поперечные сшивки между мономерами фибрина при помощи ковалентных изопептидных связей.
30.8.Особенности метаболизма эритроцита.
30.8.1. Эритроциты - высокоспециализированные клетки, основной функцией которых является транспорт кислорода из лёгких в ткани. Продолжительность жизни эритроцитов составляет в среднем 120 суток; разрушение их происходит в клетках ретикуло-эндотелиальной системы. В отличие от большинства клеток организма, у эритроцита отсутствуют клеточное ядро, рибосомы и митохондрии.
30.8.2. Энергетический обмен. Основным энергетическим субстратом эритроцита является глюкоза, которая поступает из плазмы крови путём облегчённой диффузии. Около 90% используемой эритроцитом глюкозы подвергается гликолизу(анаэробному окислению) с образованием конечного продукта - молочной кислоты (лактата). Запомните функции, которые выполняет гликолиз в зрелых эритроцитах:
1) в реакциях гликолиза образуется АТФ путём субстратного фосфорилирования. Основное направление использования АТФ в эритроцитах - обеспечение работы Na+,K+-АТФазы. Этот фермент осуществляет транспорт ионов Nа+ из эритроцитов в плазму крови, препятствует накоплению Na+ в эритроцитах и способствует сохранению геометрической формы этих клеток крови (двояковогнутый диск).
2) в реакции дегидрирования глицеральдегид-3-фосфата в гликолизе образуется НАДН. Этот кофермент является кофактором фермента метгемоглобинредуктазы, участвующей в восстановлении метгемоглобина в гемоглобин по следующей схеме:
![]()
Эта реакция препятствует накоплению метгемоглобина в эритроцитах.
3) метаболит гликолиза 1,3-дифосфоглицерат способен при участии фермента дифосфоглицератмутазы в присутствии 3-фосфоглицерата превращаться в 2,3-дифосфоглицерат:
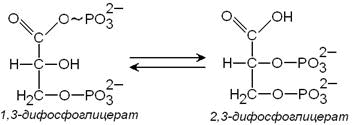
2,3-Дифосфоглицерат принимает участие в регуляции сродства гемоглобина к кислороду. Его содержание в эритроцитах повышается при гипоксии. Гидролиз 2,3-дифосфоглицерата катализирует фермент дифосфоглицератфосфатаза.
Приблизительно 10% глюкозы, потребляемой эритроцитом, используется в пентозофосфатном пути окисления. Реакции этого пути служат основным источником НАДФН для эритроцита. Данный кофермент необходим для перевода окисленного глутатиона (см. 30.8.3) в восстановленную форму. Дефицит ключевого фермента пентозофосфатного пути - глюкозо-6-фосфатдегидрогеназы - сопровождается уменьшением в эритроцитах отношения НАДФН/НАДФ+, увеличением содержания окисленной формы глутатиона и снижением резиcтентности клеток (гемолитическая анемия).
30.8.3. Механизмы обезвреживания активных форм кислорода в эритроцитах. Молекулярный кислород в определённых условиях может превращаться в активные формы, к которым относятся супероксидный анион О2-, пероксид водорода Н2О2, гидроксильный радикал ОН. и синглетный кислород 1О2. Эти формы кислорода обладают высокой реакционной способностью, могут оказывать повреждающее действие на белки и липиды биологических мембран, вызывать разрушение клеток. Чем выше содержание О2, тем больше образуется его активных форм. Поэтому эритроциты, постоянно взаимодействующие с кислородом, содержат эффективные антиоксидантные системы, способные обезвреживать активные метаболиты кислорода.
Важным компонентом антиоксидантных систем является трипептид глутатион, образующийся в эритроцитах в результате взаимодействия γ-глутамилцистеина и глицина:
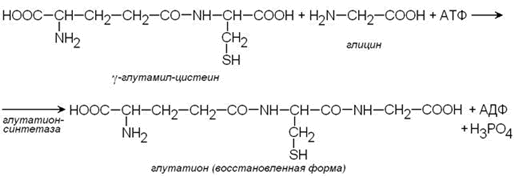
Восстановленная форма глутатиона (сокращённое обозначение Г-SH) участвует в реакциях обезвреживания пероксида водорода и органических пероксидов (R-O-OH). При этом образуются вода и окисленный глутатион (сокращённое обозначение Г-S-S-Г).

Превращение окисленного глутатиона в восстановленный катализирует фермент глутатионредуктаза. Источник водорода - НАДФН (из пентозофосфатного пути, см. 30.8.2):
![]()
В эритроцитах имеются также ферменты супероксиддисмутаза и каталаза, осуществляющие следующие превращения:

Антиоксидантные системы имеют для эритроцитов особое значение, так как в эритроцитах не происходит обновления белков путём синтеза.
ОБНОВЛЕНИЯ
ПОДПИСАТЬСЯ НА РАССЫЛКУ
ПРЕДМЕТЫ
- Анатомия
- Акушерство и гинекология
- БЖД, медицина катастроф
- Биохимия
- Биология
- Гистология
- Гигиена
- Генетика
- Диетология
- Дерматовенерология
- Инфекционные болезни
- Культурология
- Лабораторная диагностика
- Летняя практика
- Лучевая диагностика
- Медицинская информатика
- Микробиология
- Неврология
- Общественное здоровье
- Общий уход
О НАС
«Dendrit» - информационный портал для медицинских работников, студентов медицинских ВУЗов, исследователей и пациентов.
Ваш источник новостей и знаний о здоровье.